
科目: 來源: 題型:解答題
查看答案和解析>>
科目: 來源: 題型:解答題
查看答案和解析>>
科目: 來源: 題型:選擇題
| A. | A(g)+2B(g)?2C(g);△H1>0 | B. | A(g)+B(g)?C(g)+D(g);△H2>0 | ||
| C. | A(s)+2B(g)?C(g);△H3>0 | D. | A(s)?B(g)+C(g);△H4<0 |
查看答案和解析>>
科目: 來源: 題型:選擇題
| A. | 高溫、低壓 | B. | 適宜的溫度、高壓、催化劑 | ||
| C. | 低溫、低壓 | D. | 低溫、高壓、催化劑 |
查看答案和解析>>
科目: 來源: 題型:實驗題
| 銀鹽 性質 | AgCl | AgBr | AgCN | Ag2CrO4 | AgSCN |
| 顏色 | 白 | 淺黃 | 白 | 磚紅 | 白 |
| 溶解度(mol•L-1) | 1.34×10-6 | 7.1×10-7 | 1.1×10-8 | 6.5×10-5 | 1.0×10-6 |
查看答案和解析>>
科目: 來源: 題型:實驗題
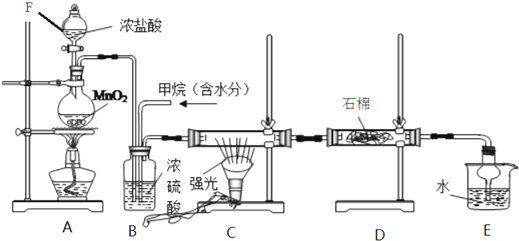
查看答案和解析>>
科目: 來源: 題型:實驗題
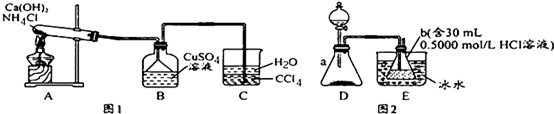
查看答案和解析>>
科目: 來源: 題型:實驗題
 酯是重要的有機合成中間體,廣泛應用于溶劑、增塑劑、香料、黏合劑及印刷、紡織等工業.乙酸乙酯的實驗室和工業制法常采用如下反應:CH3COOH+C2H5OH$?_{△}^{濃H_{2}SO_{4}}$CH3COOC2H5+H2O,請根據要求回答下列問題:
酯是重要的有機合成中間體,廣泛應用于溶劑、增塑劑、香料、黏合劑及印刷、紡織等工業.乙酸乙酯的實驗室和工業制法常采用如下反應:CH3COOH+C2H5OH$?_{△}^{濃H_{2}SO_{4}}$CH3COOC2H5+H2O,請根據要求回答下列問題:| 同一反應時間 | 同一反應溫度 | |||||
| 反應溫度/℃ | 轉化率(%) | 選擇性(%)* | 反應時間/h | 轉化率(%) | 選擇性(%)* | |
| 40 | 77.8 | 100 | 2 | 80.2 | 100 | |
| 60 | 92.3 | 100 | 3 | 87.8 | 100 | |
| 80 | 92.6 | 100 | 4 | 92.3 | 100 | |
| 120 | 94.5 | 98.7 | 6 | 93.0 | 100 | |
查看答案和解析>>
科目: 來源: 題型:實驗題
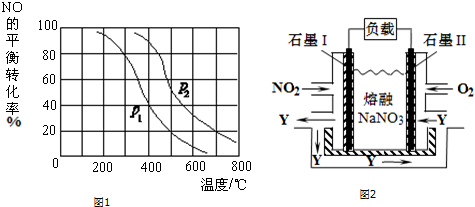
查看答案和解析>>
科目: 來源: 題型:實驗題

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com