
科目: 來源: 題型:實驗題
查看答案和解析>>
科目: 來源: 題型:填空題
查看答案和解析>>
科目: 來源: 題型:實驗題
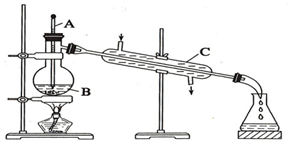 工業上通常用工業酒精和生石灰混合蒸餾法制取無水乙醇.如圖是實驗室中模擬工業原理制取無水乙醇的裝置.回答下列問題
工業上通常用工業酒精和生石灰混合蒸餾法制取無水乙醇.如圖是實驗室中模擬工業原理制取無水乙醇的裝置.回答下列問題查看答案和解析>>
科目: 來源: 題型:解答題

查看答案和解析>>
科目: 來源: 題型:實驗題
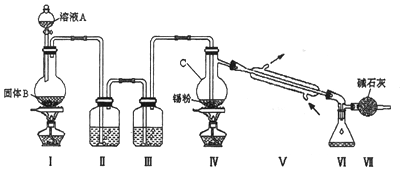
查看答案和解析>>
科目: 來源: 題型:解答題
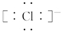 .Al在元素周期表最中的位置是第三周期第IIIA族.
.Al在元素周期表最中的位置是第三周期第IIIA族.查看答案和解析>>
科目: 來源: 題型:解答題
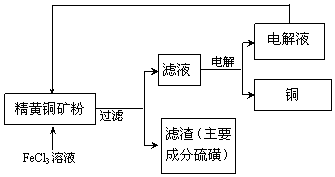
查看答案和解析>>
科目: 來源: 題型:實驗題
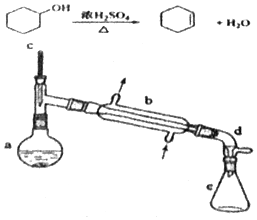 分離提純是化學實驗中的重要部分,方法有過濾、蒸發、萃取、蒸餾等,應用廣泛,環己醇 脫水是合成環己烯的常用方法,實驗室合成壞己烯的反應和實驗裝置如圖:
分離提純是化學實驗中的重要部分,方法有過濾、蒸發、萃取、蒸餾等,應用廣泛,環己醇 脫水是合成環己烯的常用方法,實驗室合成壞己烯的反應和實驗裝置如圖:| 相對分子質量 | 密度/(g•cm-3) | 沸點/℃ | 溶解性 | |
| 環己醇 | 100 | 0.9618 | 161 | 微溶于水 |
| 環己烯 | 82 | 0.8102 | 83 | 難溶于水 |
查看答案和解析>>
科目: 來源: 題型:實驗題
查看答案和解析>>
科目: 來源: 題型:實驗題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com