
分析 ①依據配制溶液體積選擇合適的容量瓶,依據m=CVM計算需要溶質的質量;
②依據配制一定物質的量濃度溶液一般步驟選擇需要儀器;
③分析操作對溶質的物質量和溶液體積的影響,依據C=$\frac{n}{V}$進行誤差分析;
④配制一定物質的量濃度溶液一般步驟:計算、稱量、溶解、冷卻、移液、洗滌、定容、搖勻、裝瓶、貼標簽,據此排序.
解答 解:①配制150mL 0.2mol•L-1NaOH溶液,應選擇250mL容量瓶,需要氫氧化鈉的質量m=0.2mol/L×40g/mol×0.25L=2.0g;
故答案為:2.0;
②配制一定物質的量濃度溶液一般步驟:計算、稱量、溶解、冷卻、移液、洗滌、定容、搖勻等,用到的儀器:托盤天平、藥匙、燒杯、玻璃棒、250mL容量瓶、膠頭滴管;
故答案為:托盤天平、藥匙、燒杯、玻璃棒、250mL容量瓶、膠頭滴管;
③A.將NaOH放在紙張上稱量,導致稱取的溶質質量偏小,溶質的物質的量偏小,溶液濃度偏低,故A不選;
B.定容時俯視刻度線,導致溶液體積偏小,溶液濃度偏高,故B選;
C.定容時仰視刻度線,導致溶液體積偏大,溶液濃度偏低,故C不選;
D.容量瓶用蒸餾水洗滌后未干燥即用來配制溶液,對溶質的物質的量和溶液體積都不產生影響,溶液濃度不變,故D不選;
故選:B;
④配制一定物質的量濃度溶液一般步驟:計算、稱量、溶解、冷卻、移液、洗滌、定容、搖勻、裝瓶、貼標簽,所以正確的順序為:BCAFED;
故答案為:BCAFED.
點評 本題考查了一定物質的量濃度溶液的配制,明確配制原理及操作步驟是解題關鍵,注意誤差分析的方法和技巧,題目難度不大.


科目:高中化學 來源: 題型:填空題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
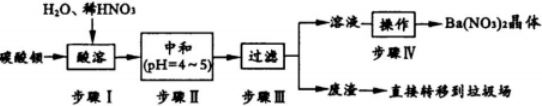
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
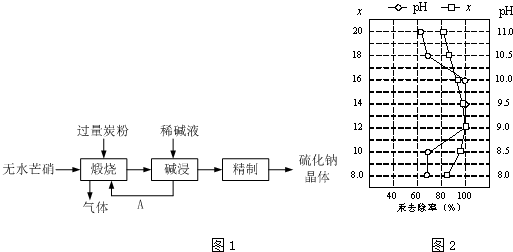
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
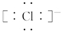 .Al在元素周期表最中的位置是第三周期第IIIA族.
.Al在元素周期表最中的位置是第三周期第IIIA族.查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①⑤ | B. | ③④ | C. | ② | D. | 全都不行 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Na+、Cu2+、Cl-、SO42- | B. | Na+、HCO3-、Cl-、NO3- | ||
| C. | Na+、SO32-、NO3-、K+ | D. | K+、SO42-、Mg2+、Cl- |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com