
科目: 來源: 題型:選擇題
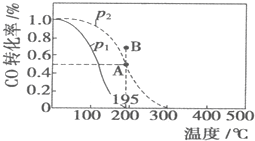 在20L恒容密閉容器中,按物質的量之比為1:2充入CO和H2發生:CO(g)+2H2(g)?CH3OH(g)△H=akJ/mol.測得CO的轉化率隨溫度及不同壓強的變化如圖所示:n(H2)在P2及195℃時隨時間變化如表所示
在20L恒容密閉容器中,按物質的量之比為1:2充入CO和H2發生:CO(g)+2H2(g)?CH3OH(g)△H=akJ/mol.測得CO的轉化率隨溫度及不同壓強的變化如圖所示:n(H2)在P2及195℃時隨時間變化如表所示| t/min | 0 | 1 | 3 | 5 |
| n(H2)/mol | 8 | 5 | 4 | 4 |
| A. | P1>P2,a<0 | |
| B. | 在P2及195℃時,反應前3min的平均速率v(CH3OH)=0.08mol/(L•min) | |
| C. | 在P2及195℃時,該反應的平衡常數為25(mol/L)-2 | |
| D. | 在B點時,v正>v逆 |
查看答案和解析>>
科目: 來源: 題型:選擇題
| 物質 | X | Y | Z |
| 初始濃度/mol•L-1 | 0.1 | 0.2 | 0 |
| 2 min末濃度/mol•L-1 | 0.08 | a | b |
| 平衡濃度/mol•L-1 | 0.05 | 0.05 | 0.1 |
| A. | 平衡時,X 的轉化率為20% | |
| B. | t℃時,該反應的平衡常數為40 | |
| C. | 增大平衡后的體系壓強,v正增大,v逆減小,平衡向正反應方向移動 | |
| D. | 前2 min 內,用Y 的變化量表示的平均反應速率v(Y)=0.03 mol•L-1•min-1 |
查看答案和解析>>
科目: 來源: 題型:實驗題
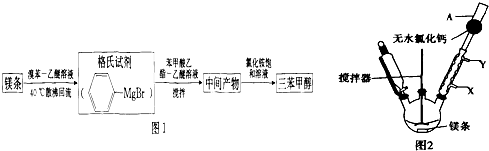
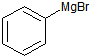 +H2O→
+H2O→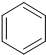 +Mg(OH)Br(堿式溴化鎂)
+Mg(OH)Br(堿式溴化鎂)| 物質 | 熔點 | 沸點 | 溶解性 |
| 三苯甲醇 | 164.2℃ | 380℃ | 不溶于水,溶于乙醇、乙醚等有機溶劑 |
| 乙醚 | -116.3℃ | 34.6℃ | 微溶于水,溶于乙醇、苯等有機溶劑 |
| 溴苯 | -30.7℃ | 156.2℃ | 不溶于水,溶于乙醇、乙醚等多數有機溶劑 |
| 苯甲酸乙酯 | -34.6℃ | 212.6℃ | 不溶于水 |
| Mg(OH)Br | 常溫下為固體 | 能溶于水,不溶于醇、醚等有機溶劑 | |
查看答案和解析>>
科目: 來源: 題型:實驗題
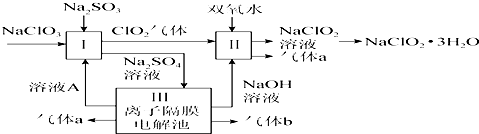
查看答案和解析>>
科目: 來源: 題型:解答題
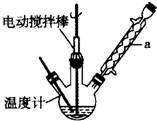
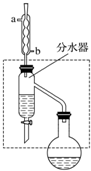 乙酸丁酯是重要的化工原料,具有水果香味.實驗室制備乙酸丁酯的反應、裝置示意圖和有關信息如下:CH3COOH+CH3CH2CH2CH2OH$?_{△}^{濃H_{2}SO_{4}}$ CH3COOCH2CH2CH2CH3+H2O
乙酸丁酯是重要的化工原料,具有水果香味.實驗室制備乙酸丁酯的反應、裝置示意圖和有關信息如下:CH3COOH+CH3CH2CH2CH2OH$?_{△}^{濃H_{2}SO_{4}}$ CH3COOCH2CH2CH2CH3+H2O| 乙酸 | 正丁醇 | 乙酸丁酯 | |
| 熔點/℃ | 16.6 | -89.5 | -73.5 |
| 沸點/℃ | 117.9 | 117 | 126.0 |
| 密度/g•cm-3 | 1.1 | 0.80 | 0.88 |
查看答案和解析>>
科目: 來源: 題型:實驗題
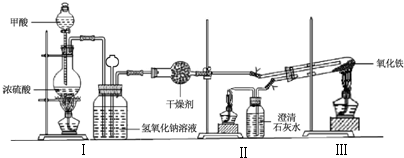
| 加熱方式 | 產物元素組成 | 各元素的質量分數% | |
| Fe | O | ||
| 酒精燈 | Fe和O | 74.50 | 25.50 |
| 帶網罩酒精燈 | Fe和O | 76.48 | 23.52 |
| 酒精噴燈 | Fe | 100.00 | 0.00 |
查看答案和解析>>
科目: 來源: 題型:實驗題
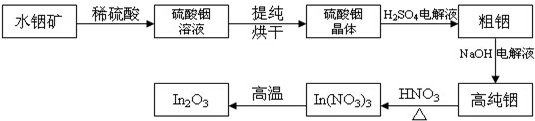
查看答案和解析>>
科目: 來源: 題型:選擇題
| A. | 10% | B. | 25% | C. | 50% | D. | 67% |
查看答案和解析>>
科目: 來源: 題型:選擇題
| A. | v(C)=0.5mol/(L•min) | |
| B. | x=3 | |
| C. | B的轉化率為25% | |
| D. | 若使用催化劑可以縮短達到平衡的時間,但A轉化率不變 |
查看答案和解析>>
科目: 來源: 題型:實驗題
 甲苯(
甲苯(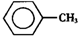 )是一種重要的化工原料,能用于生產苯甲醛(
)是一種重要的化工原料,能用于生產苯甲醛(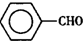 )、苯甲酸(
)、苯甲酸(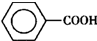 )等產品.下表列出了有關物質的部分物理性質,請回答:
)等產品.下表列出了有關物質的部分物理性質,請回答:| 稱 | 性狀 | 熔點(℃) | 沸點(℃) | 相對密度(ρ水=1g/cm3) | 溶解性 | |
| 水 | 乙醇 | |||||
| 甲苯 | 無色液體易燃易揮發 | -95 | 110.6 | 0.8660 | 不溶 | 互溶 |
| 苯甲醛 | 無色液體 | -26 | 179 | 1.0440 | 微溶 | 互溶 |
| 苯甲酸 | 白色片狀或針狀晶體 | 122.1 | 249 | 1.2659 | 微溶 | 易溶 |
 ,此反應的原子利用率理論上可達66.25%.
,此反應的原子利用率理論上可達66.25%.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com