
科目: 來源: 題型:選擇題
| A. | 人類目前所利用的能量大部分是由化學反應產生的 | |
| B. | 煤、石油、天然氣是當今世界最重要的三種化石燃料 | |
| C. | 我國目前最主要的能源是石油 | |
| D. | 能量變化是化學反應的基本特征之一 |
查看答案和解析>>
科目: 來源: 題型:選擇題
| A. | 溫室效應 | B. | 氮的氧化物排放 | C. | 白色污染 | D. | 對臭氧層的破壞 |
查看答案和解析>>
科目: 來源: 題型:選擇題
| A. | 有毒的 | B. | 單質 | C. | 氧化物 | D. | 金屬或合金 |
查看答案和解析>>
科目: 來源: 題型:選擇題
| A. | 工業廢水經處理達標后再排放 | B. | 農業生產中農藥、化肥正確使用 | ||
| C. | 禁止使用化肥、農藥 | D. | 城市垃圾妥善處理 |
查看答案和解析>>
科目: 來源: 題型:選擇題
| A. | (a+0.5b-1.5c) kJ•mol-1 | B. | (a-0.5b+1.5c) kJ•mol-1 | ||
| C. | (2a+b-3c) kJ•mol-1 | D. | (2a+b+3c) kJ•mol-1 |
查看答案和解析>>
科目: 來源: 題型:實驗題
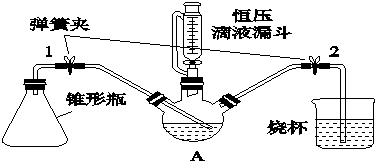
查看答案和解析>>
科目: 來源: 題型:實驗題
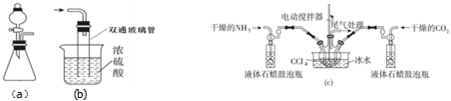
查看答案和解析>>
科目: 來源: 題型:實驗題

查看答案和解析>>
科目: 來源: 題型:實驗題
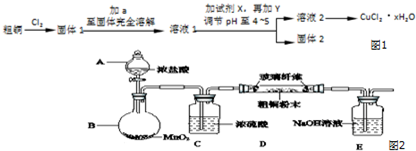
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com