
科目: 來源: 題型:解答題
查看答案和解析>>
科目: 來源: 題型:解答題
| 溫度/℃ | 25 | T2 |
| 水的離子積常數 | 1×10-14 | 1×10-12 |
| 難溶物 | Fe(OH)2 | Fe(OH)3 | Zn(OH)2 |
| Ksp | 8.0×10-16 | 8.0×10-38 | 1.0×10-17 |
查看答案和解析>>
科目: 來源: 題型:解答題
查看答案和解析>>
科目: 來源: 題型:選擇題
| A. | A的金屬性強于B | |
| B. | 電子不斷由A電極經外電路流向B電極 | |
| C. | A電極上發生的電極反應是還原反應 | |
| D. | A的金屬活動性一定排在氫前面 |
查看答案和解析>>
科目: 來源: 題型:解答題
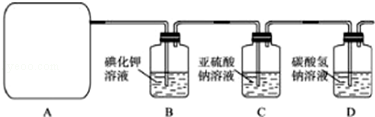

查看答案和解析>>
科目: 來源: 題型:解答題
查看答案和解析>>
科目: 來源: 題型:解答題
查看答案和解析>>
科目: 來源: 題型:解答題
 某廢金屬屑中主要成分為Cu、Fe、Al,還含有少量的銅銹[Cu2(OH)2CO3]、少量的鐵銹和少量的氧化鋁,用上述廢金屬屑制取膽礬(CuSO4•5H2O)、無水AlCl3和鐵紅的過程如圖所示:
某廢金屬屑中主要成分為Cu、Fe、Al,還含有少量的銅銹[Cu2(OH)2CO3]、少量的鐵銹和少量的氧化鋁,用上述廢金屬屑制取膽礬(CuSO4•5H2O)、無水AlCl3和鐵紅的過程如圖所示:查看答案和解析>>
科目: 來源: 題型:選擇題
| A. | 乙烯能使酸性高錳酸鉀溶液褪色 | |
| B. | 苯能使酸性高錳酸鉀溶液褪色 | |
| C. | 乙醇可以和金屬鈉反應放出氫氣 | |
| D. | 乙酸可以與乙醇在一定條件下發生酯化反應 |
查看答案和解析>>
科目: 來源: 題型:選擇題
| A. | 用氨水吸收少量二氧化硫:NH3•H2O+SO2═NH4++HSO3- | |
| B. | NH4HCO3溶液與過量NaOH溶液反應:NH4++OH-═NH3↑+H2O | |
| C. | 過量的鐵粉與濃硝酸反應:Fe+4H++2NO3-═Fe2++2NO2↑+2H2O | |
| D. | 向漂白粉溶液中通入適量SO2:Ca2++2C1O-+SO2+H2O═CaSO3↓+2HC1O |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com