
科目: 來源: 題型:選擇題
| A. | ①② | B. | ①④ | C. | ①③ | D. | ②③ |
查看答案和解析>>
科目: 來源: 題型:選擇題
| A. | BiONO3 | B. | (NH4)2Fe(SO4)2 | C. | Ca(ClO)Cl | D. | K3Fe(CN)6 |
查看答案和解析>>
科目: 來源: 題型:解答題
| 實驗 序號 | 實驗目的 | 初始pH | 廢水樣品體積/mL | CuSO4溶液的體積/mL | 雙氧水溶液的體積/mL | 蒸餾水的體積/mL |
| ① | 為以下實驗操作參考 | 7 | 60 | 10 | 10 | 20 |
| ② | 廢水的初始pH對破氰反應速率的影響 | 12 | 60 | 10 | 10 | 20 |
| ③ | 雙氧水的濃度對破氰反應速率的影響 | 7 | 60 | 10 | 20 | 10 |

| 實驗步驟(不要寫出具體操作過程) | 預期實驗現象和結論 |
查看答案和解析>>
科目: 來源: 題型:填空題
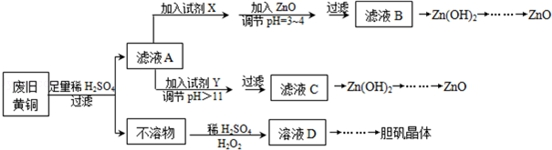
| Fe3+ | Fe2+ | Zn2+ | |
| 開始沉淀的pH | 1.1 | 5.8 | 5.9 |
| s沉淀完全的pH | 3.0 | 8.8 | 8.9 |
查看答案和解析>>
科目: 來源: 題型:填空題
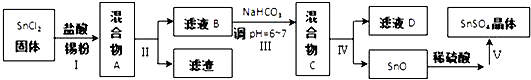
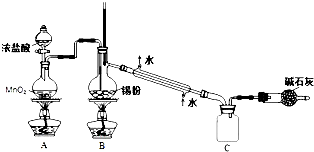
查看答案和解析>>
科目: 來源: 題型:解答題
查看答案和解析>>
科目: 來源: 題型:解答題
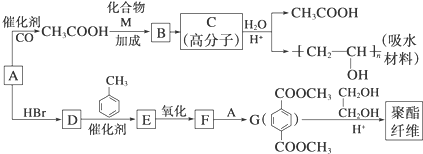
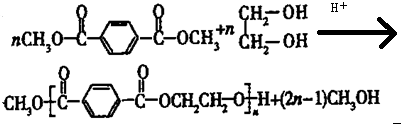 .
.查看答案和解析>>
科目: 來源: 題型:選擇題
| A. | 向稀HNO3中滴加Na2SO3溶液:SO32-+2H+═SO2↑+H2O | |
| B. | 向Na2SiO3溶液中通入過量SO2:SiO32-+SO2+H2O═H2SiO3↓+SO32- | |
| C. | 向Al2(SO4)3溶液中加入過量的NH3•H2O:Al3++4 NH3•H2O═AlO2-+4NH4++2H2O | |
| D. | 向Fe(NO3)2溶液中滴加稀鹽酸:3Fe2++NO3-+4H+═3Fe3++NO↑+2H2O |
查看答案和解析>>
科目: 來源: 題型:解答題
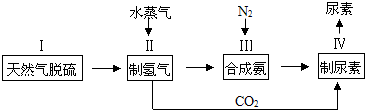
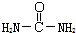 ,請寫出尿素的同分異構體中含有離子鍵的化學式NH4OCN.
,請寫出尿素的同分異構體中含有離子鍵的化學式NH4OCN.查看答案和解析>>
科目: 來源: 題型:解答題

查看答案和解析>>
湖北省互聯(lián)網違法和不良信息舉報平臺 | 網上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com