
科目: 來源:2015-2016學年浙江省桐鄉市高二上期中(普通班)化學試卷(解析版) 題型:選擇題
在一密閉容器中,反應aA(g)  bB(g)達到平衡后,保持溫度不變,將容器體積增大一倍,當達到新平衡時,B的濃度是原來的60%,則
bB(g)達到平衡后,保持溫度不變,將容器體積增大一倍,當達到新平衡時,B的濃度是原來的60%,則
A.平衡向逆反應方向移動了 B.物質A的轉化率減小了
C.物質B的質量分數增加了 D.a>b
查看答案和解析>>
科目: 來源:2015-2016學年浙江省桐鄉市高二上期中(普通班)化學試卷(解析版) 題型:選擇題
在容積為2L的密閉容器中進行反應:CO(g)+2H2(g) CH3OH(g) ,其他條件不變,在300℃和500℃時,物質的量n(CH3OH)-反應時間t的變化曲線如圖所示,下列說法正確的是
CH3OH(g) ,其他條件不變,在300℃和500℃時,物質的量n(CH3OH)-反應時間t的變化曲線如圖所示,下列說法正確的是

A.該反應的△H>0
B.其他條件不變,升高溫度反應的平衡常數增大
C.300℃時,0-t1min內 CH3OH的平均生成速率為n1/2t1 mol·L-1 min-1
D.A點的反應體系從300℃升高到500℃,達到平衡時n(H2)/n(CH3OH)減小
查看答案和解析>>
科目: 來源:2015-2016學年浙江省桐鄉市高二上期中(普通班)化學試卷(解析版) 題型:實驗題
取6根鐵釘,6支干凈的試管及其他材料,如圖所示。

試管①放入一根鐵釘,再注入蒸餾水,使鐵釘和空氣及水接觸;
試管②在試管底部放入硅膠(是一種干燥劑),再放入鐵釘,用棉花團堵住試管口,使鐵釘和干燥空氣接觸;
試管③先放入一根鐵釘,趁熱倒入煮沸的蒸餾水(已趕出原先溶解在蒸餾水中的空氣)浸沒鐵釘,再加上一層植物油,使鐵釘不能跟空氣接觸;
試管④中放入鐵釘注入食鹽水,使鐵釘和空氣及食鹽水接觸;
試管⑤放入相連的鐵釘和鋅片,注入自來水,浸沒鐵釘和鋅片;
試管⑥放入相連的鐵釘和銅絲,注入自來水,浸沒鐵釘和銅絲。
把6支試管放在試管架上,幾天后觀察鐵釘被腐蝕的情況。
(1)上述實驗中鐵釘發生了電化學腐蝕的是____ (填試管序號);在電化學腐蝕中,負極反應是__________。
(2)從鐵釘被腐蝕的情況可知引起和促 進鐵釘被腐蝕的條件是___________。
進鐵釘被腐蝕的條件是___________。
(3)為防止鐵的銹蝕,工業上普遍采用的方法是_______(答兩種方法)。
查看答案和解析>>
科目: 來源:2015-2016學年浙江省桐鄉市高二上期中(普通班)化學試卷(解析版) 題型:填空題
碳、氮及其化 合物在工農業生產生活中有著重要作用。請回答下列問題:
合物在工農業生產生活中有著重要作用。請回答下列問題:
(1)用CH4 催化還原NOx 可以消除氮氧化物的污染。例如:
CH4(g) + 4NO2(g) = 4NO(g)+CO2(g) + 2H2O(g) ΔH1=-574 kJ·mol-1
CH4(g) + 4NO(g) = 2 N2(g)+CO2(g) + 2H2O(g) ΔH2
若2 mol CH4 還原NO2 至N2,整個過程中放出的熱量為1734 kJ,則ΔH2= ;
(2)據報道 ,科學家在一定條件下利用Fe2O3與甲烷反應可制取“納米級”的金屬鐵。其反應如下: Fe2O3(s) + 3CH4(g)
,科學家在一定條件下利用Fe2O3與甲烷反應可制取“納米級”的金屬鐵。其反應如下: Fe2O3(s) + 3CH4(g)  2Fe(s) + 3CO(g) +6H2(g) ΔH>0
2Fe(s) + 3CO(g) +6H2(g) ΔH>0
① 若反應在5L的密閉容器中進行,1min后達到平衡,測得Fe2O3在反應中質量減少3.2g。則該段時間內CO的平均反應速率為 _________ 。
② 若該反應在恒溫恒壓容器中進行,能表明該反應達到平衡狀態的是_____(選填序號)
a.CH4的轉化率等于 CO的產率
CO的產率
b.混合氣體的平均相對分子質量不變
c.v(CO)與v(H2)的比值不變
d.固體的總質量不變
③ 該反應達到平衡時某物理量隨溫度變化如圖所示,當溫度由T1升高到T2時,平衡常數KA____KB(填“>”、“ <”或“=”)。縱坐標可以表示的物理量有哪些 。
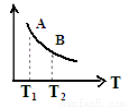
a.H2的逆反應速率
b.CH4的的體積分數
c.混合氣體的平均相對分子質量
查看答案和解析>>
科目: 來源:2015-2016學年浙江省高二上學期第一次質檢化學試卷(解析版) 題型:選擇題
未來新能源的特點是資源豐富,在使用時對環境無污染或污染很小,且可以再生。下列屬于未來新能源標準的是
①天然氣 ②煤 ③核能 ④石油 ⑤太陽能
A.⑤ B.①③⑤ C.③⑤ D.①②④
查看答案和解析>>
科目: 來源:2015-2016學年浙江省高二上學期第一次質檢化學試卷(解析版) 題型:選擇題
在2A+B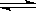 3C+4D反應中,表示該反應速率最快的是
3C+4D反應中,表示該反應速率最快的是
A.υ(A)= 0.5 mol/(L·s) B.υ(B)= 0.3 mol/(L·s)
C.υ(C)= 0.8 mol/(L·s) D.υ(D)= 1 mol/(L·s)
查看答案和解析>>
科目: 來源:2015-2016學年浙江省高二上學期第一次質檢化學試卷(解析版) 題型:選擇題
下列有關熱化學方程式的敘述正確的是
A.已知2H2(g)+O2(g)=2H2O(g);△H=-483.6kJ/mol,則氫氣的燃燒熱為241.8 kJ/mol
B.已知C(石墨,s)=C(金剛石,s);△H>0,則金剛石比石墨穩定
C.含20.0g NaOH的稀溶液與稀鹽酸完全中和,放出28.7kJ的熱量,則表示該反應中和熱的熱化學方程式為:NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l);△H=-57.4kJ/mol
D.己知2C(s)+2O2(g)=2CO2(g);△H1 2C(s)+O2(g)=2CO(g);△H2 則△H1>△H2
查看答案和解析>>
科目: 來源:2015-2016學年浙江省高二上學期第一次質檢化學試卷(解析版) 題型:實驗題
I、某學生實驗小組用50mL0.50mol•L—1的鹽酸與50mL0.50mol•L—1的NaOH溶液在右圖所示的裝置中進行中和反應反應熱的測定
(1)圖中裝置缺少的一種儀器,該儀器名稱為 。

(2)將反應混合液的 溫度記為反應的終止溫度。
(3)下列說法正確的是
A.小燒杯內殘留有水,會使測得的反應熱數值偏小
B.可用相同濃度和體積的醋酸代替稀鹽酸溶液進行實驗
C.燒杯間填滿碎紙條的作用是固定小燒杯
D.酸、堿混合時,應把量筒中的溶液緩緩倒入燒杯的溶液中,以防液體外濺
II、某實驗小組以H2O2分解為例,研究濃度、催化劑、溶液酸堿性對反應速率的影響。在常溫下按照如下方案完成實驗。
實驗編號 | 反應物 | 催化劑 |
① | 10mL2% H2O2溶液 | 無 |
② | 10mL5% H2O2溶液 | 無 |
③ | 10mL5% H2O2溶液 | 1mL0.1mol·L-1FeCl3溶液 |
④ | 10mL5% H2O2溶液+少量HCl溶液 | 1mL0.1mol·L-1FeCl3溶液 |
⑤ | 10mL5% H2O2溶液+少量NaOH溶液 | 1mL0.1mol·L-1FeCl3溶液 |
(1)催化劑能加快化學反應速率的原因是__________________。
(2)實驗①和②的目的是____________________________。實驗時由于較長時間沒有觀察到明顯現象而無法得出結論。資料顯示,通常條件下H2O2穩定,不易分解。為了達到實驗目的,你對原實驗方案的改進是____________________。
(3)寫出實驗③的化學反應方程式 。
(4)實驗③、④、⑤中,測得生成氧氣的體積隨時間變化的關系如下圖。

分析上圖能夠得出的實驗結論是_______________________。
查看答案和解析>>
科目: 來源:2015-2016學年浙江省高一上學期12月月考化學試卷(解析版) 題型:選擇題
下列物質中屬于堿的是
A.CH4(甲烷) B.CH3COOH(醋酸) C.H2SO4 D.KOH
查看答案和解析>>
科目: 來源:2015-2016學年浙江省高一上學期12月月考化學試卷(解析版) 題型:選擇題
224mL某氣體在標準狀況下的質量為0.32g,該氣體的摩爾質量約為
A.32g·mol-1 B.32 C.64g·mol-1 D.64
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com