
科目: 來源:2015-2016學年四川省雅安市高一上學期12月月考化學試卷(解析版) 題型:填空題
Ⅰ.在MgCl2溶液中滴入NaOH溶液,會有白色沉淀出現,該白色沉淀不能溶解于過量的氫氧化鈉中。反應的離子方程式是 ;但Al(OH)3卻能溶解在過量NaOH溶液中,該反應的離子方程式是 。
Ⅱ.在含有0.4molHCl和0.1molMgSO4的混合溶液中逐滴加入Ba(OH)2 溶液,產生的沉淀質量m與加入Ba(OH)2的物質的量n之間的關系如圖所示。
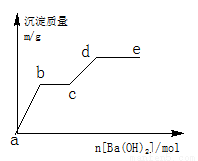
(1)a→b過程中發生反應的離子方程式是
(2)b→c發生反應的離子方程式是
(3)d點沉淀質量是 g。
查看答案和解析>>
科目: 來源:2015-2016學年山東省平度市高一上學期直升班抽考化學試卷(解析版) 題型:選擇題
下列物質中屬于電解質,且能導電的是
A.熔融的氫氧化鉀 B.液態銅
C.液態氯化氫 D.固態氯化鉀
查看答案和解析>>
科目: 來源:2015-2016學年山東省平度市高一上學期直升班抽考化學試卷(解析版) 題型:選擇題
設NA為阿伏加德羅常數的值,下列說法中正確的是
A.128gC60中含有90NA個分子
B.46g NO2和N2O4的混合氣體含有的原子數為3NA
C.標準狀況下,22.4L CCl4所含的分子數為6.02×1023
D.100mL0.1 mol·L-1CaCl2溶液中Cl-的物質的量濃度為0.01 mol·L-1
查看答案和解析>>
科目: 來源:2015-2016學年山東省平度市高一上學期直升班抽考化學試卷(解析版) 題型:選擇題
下列反應中,Na2O2只表現出氧化性的是
A.2Na2O2+2H2O=4NaOH+O2↑
B.2Na2O2+2H2SO4=2Na2SO4+2H2O+O2↑
C.Na2O2+SO2=Na2SO4
D.5Na2O2+2KMnO4+8H2SO4=SNa2SO4+K2SO4+2MnSO4+5O2↑+8H2O
查看答案和解析>>
科目: 來源:2015-2016學年山東省平度市高一上學期直升班抽考化學試卷(解析版) 題型:選擇題
將12 mol·L-1的鹽酸(ρ=1.15g/cm3)50mL稀釋成6mol·L-1的鹽酸(ρ=1.10g/cm3),需加水的體積為
A.57.5mL B.55mL C.52.5mL D.50mL
查看答案和解析>>
科目: 來源:2015-2016學年山東省平度市高一上學期直升班抽考化學試卷(解析版) 題型:實驗題
氫化鈣固體是登山運動員常用的能源提供劑。某興趣小組擬選用如下裝置制備氫化鈣。
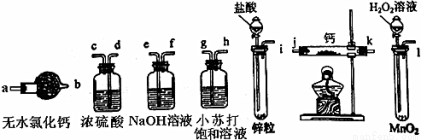
請回答下列問題:
(1)寫出該實驗中產生氫氣的離子方程式并用單線橋表示電子轉移的方向和數目:_______________。
(2)根據完整的實驗裝置進行實驗,實驗步驟如下:檢查裝置氣密性后,裝入藥品;打開分液漏斗活塞_________(請按正確的順序填入下列步驟的標號)。
A.加熱反應一段時間 B.收集氣體并檢驗其純度
C.關閉分液漏斗活塞 D.停止加熱,充分冷卻
(3)請選擇必要的裝置,按氣流方向連接順序為________________(填儀器接口的字母編號)。
(4)實驗結束后,甲同學取少量產物,小心加入水中,觀察到有氣泡冒出,溶液中加入酚酞后顯紅色,于是甲同學判斷上述實驗中確有CaH2生成。請根據甲同學的現象寫出CaH2與水反應的化學方程式______________________。乙同學發現將單質鈣加入水中也能發生上述現象,因此乙同學認為不能證明確有CaH2產生,請你設計一個實驗,用化學方法區分鈣與氫化鈣,寫出實驗簡要步驟及觀察到的現象______________________。
查看答案和解析>>
科目: 來源:2015-2016學年山東省平度市高二上學期直升班抽考化學試卷(解析版) 題型:選擇題
對于可逆反應4NH3(g)+5O2(g)  4NO(g)+6H2O(g) ,下列敘述正確的是
4NO(g)+6H2O(g) ,下列敘述正確的是
A. 達到化學平衡狀態時,4v正(O2)=5V逆(NO)
B. 化學反應速率的關系為2V正(NH3)=3V正(H2O)
C. 達到化學平衡狀態時,若增加容器體積,則正反應速率減小,逆反應速率增大
D. 若單位時間內生成xmolNO的同時,消耗xmolNH3,則反應達到化學平衡狀態
查看答案和解析>>
科目: 來源:2015-2016學年山東省平度市高二上學期直升班抽考化學試卷(解析版) 題型:選擇題
可逆反應mA(g) nB(g)+pC(s);△H=Q, 溫度和壓強的變化對正、逆反應速率的影響分別符合下圖中的兩個圖像,以下敘述正確的是
nB(g)+pC(s);△H=Q, 溫度和壓強的變化對正、逆反應速率的影響分別符合下圖中的兩個圖像,以下敘述正確的是

A.m>n, Q<0 B.m>n+p,Q>0
C.m>n, Q>0 D.m<n+p, Q <0
查看答案和解析>>
科目: 來源:2015-2016學年山東省平度市高二上學期直升班抽考化學試卷(解析版) 題型:選擇題
已知各物質的溶度積:Ksp (FeS) =6.3×10-18mol2·L-2 , Ksp (CuS) =1.3×10-36mol2·L-2
下列說法正確的是
A.同溫度下,CuS的溶解度大于FeS的溶解度
B.同溫度下,向飽和FeS溶液中加入少量Na2S固體后,Ksp(FeS)變小
C.向含有等物質的量的FeCl2和CuCl2的混合溶液中逐滴加入Na2S溶液,最先出現的沉淀是FeS
D.除去工業廢水中的Cu2+,可以選用FeS做沉淀劑
查看答案和解析>>
科目: 來源:2015-2016學年山東省平度市高二上學期直升班抽考化學試卷(解析版) 題型:填空題
Ⅰ、下圖表示了298K時氮氣與氫氣合成氨反應過程中的能量變化,據此請回答:
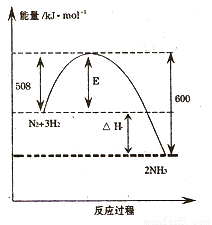
(1)寫出氮氣與氫氣合成氨的熱化學反應方程式: 。
(2)已知在常溫常壓下:
2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) ΔH =-a kJ·mol-1
2CO(g)+O2(g)=2CO2(g) ΔH =-b kJ·mol-1
H2O(g)= H2O(l) ΔH=-c kJ·mol-1
則,CH3OH(l)+O2(g) =CO(g)+2H2O(l) ΔH=______________kJ·mol-1。
Ⅱ、25℃時,取0.1mol/LHA溶液與0.1mol/LNaOH溶液等體積混合(混合后溶液體積的變化不計),測得混合溶液的pH=8,試回答以下問題:
(1)混合溶液的pH=8的原因是 (用離子方程式表示) 。
(2)混合溶液中由水電離出的[H+]_______________0.1mol/LNaOH溶液中由水電離出的[H+] (填“>”、“<”、或“=”) 。
(3)求出混合液中下列算式的計算結果(填具體數字):[HA]+[A-]= mol·L-1
(4)混合溶液中[Na+]、[H+]、[A-]、[OH-]、[HA]微粒濃度的由大到小順序為 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com