
科目: 來源:2014年高考化學一輪復習課后規范訓練7-2練習卷(解析版) 題型:選擇題
下列各組物質的變化不能用勒夏特列原理解釋的是( )
A.氯水在光照條件下顏色變淺最終變為無色
B.將FeS固體投入到含有Cu2+的廢水中以除去Cu2+
C.500 ℃時比室溫更利于合成氨
D.乙酸乙酯的合成中用濃硫酸比稀硫酸更有利于乙酸乙酯的生成
查看答案和解析>>
科目: 來源:2014年高考化學一輪復習課后規范訓練7-2練習卷(解析版) 題型:選擇題
為了探究外界條件對反應aX(g)+bY(g)  cZ(g)的影響,以X和Y物質的量之比為a∶
cZ(g)的影響,以X和Y物質的量之比為a∶
b開始反應,通過實驗得到不同條件下達到平衡時Z的體積分數,實驗結果如下圖所示。以下判斷正確的是( )
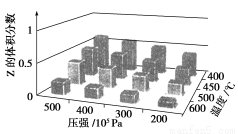
A.ΔH>0,a+b>c B.ΔH>0,a+b<c
C.ΔH<0,a+b>c D.ΔH<0,a+b<c
查看答案和解析>>
科目: 來源:2014年高考化學一輪復習課后規范訓練7-2練習卷(解析版) 題型:選擇題
在100 ℃時,將0.40 mol二氧化氮氣體充入2 L密閉容器中,每隔一段時間對該容器內
的物質進行分析,得到如下數據:
時間(s) | 0 | 20 | 40 | 60 | 80 |
n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
下列說法中正確的是( )
A.反應開始20 s內以二氧化氮表示的平均反應速率為0.001 25 mol·L-1·s-1
B.80 s時混合氣體的顏色與60 s時相同,比40 s時的顏色深
C.80 s時向容器中加入0.32 mol氦氣,同時將容器擴大為4 L,則平衡將不移動
D.若起始投料為0.20 mol N2O4,相同條件下達平衡,則各組分含量與原平衡體系對應相等
查看答案和解析>>
科目: 來源:2014年高考化學一輪復習課后規范訓練7-2練習卷(解析版) 題型:選擇題
已知一定溫度時發生反應Na2SO4(s)+4H2(g)  Na2S(s)+4H2O(g) ΔH=-225 kJ·mol-1,該反應的正反應速率隨時間的變化情況如圖所示,在t1時改變了某種條件,反應在t2時達平衡,改變的條件可能是( )
Na2S(s)+4H2O(g) ΔH=-225 kJ·mol-1,該反應的正反應速率隨時間的變化情況如圖所示,在t1時改變了某種條件,反應在t2時達平衡,改變的條件可能是( )
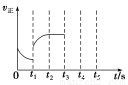
A.升高溫度 B.增大H2的濃度
C.使用催化劑 D.增大壓強
查看答案和解析>>
科目: 來源:2014年高考化學一輪復習課后規范訓練7-2練習卷(解析版) 題型:選擇題
已知CO和H2在一定條件下合成甲醇的反應為CO(g)+2H2(g)  CH3OH(g)。現在容積均為1 L的a、b、c三個密閉容器中分別充入1 mol CO和2 mol H2的混合氣體,控制溫度進行反應,測得相關數據的關系如圖所示。下列說法正確的是( )
CH3OH(g)。現在容積均為1 L的a、b、c三個密閉容器中分別充入1 mol CO和2 mol H2的混合氣體,控制溫度進行反應,測得相關數據的關系如圖所示。下列說法正確的是( )
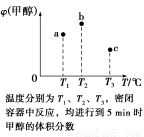
A.正反應的ΔH>0
B.反應進行到5 min時,b容器中v正=v逆
C.減壓可將b中的平衡狀態轉變成c中的平衡狀態
D.達到平衡時,a、b、c中CO的轉化率為b>a>c
查看答案和解析>>
科目: 來源:2014年高考化學一輪復習課后規范訓練7-2練習卷(解析版) 題型:選擇題
在容積一定的密閉容器中,反應A(?)+B(g)  C(g)+D(g)達到平衡后,升高溫度容器
C(g)+D(g)達到平衡后,升高溫度容器
內氣體的密度增大,則下列敘述正確的是( )
A.正反應是放熱反應
B.A不是氣態物質,加入A該平衡向正反應方向移動
C.其他條件不變,加入A平衡不移動
D.改變壓強對該平衡的移動無影響
查看答案和解析>>
科目: 來源:2014年高考化學一輪復習課后規范訓練7-2練習卷(解析版) 題型:選擇題
在某恒容的密閉容器中,可逆反應A(g)+B(g)  xC(g)有如圖所示的關系曲線,下列說法正確的是( )
xC(g)有如圖所示的關系曲線,下列說法正確的是( )
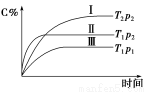
A.溫度:T1>T2 B.壓強:p1>p2
C.正反應是吸熱反應 D.x的值是2
查看答案和解析>>
科目: 來源:2014年高考化學一輪復習課后規范訓練7-2練習卷(解析版) 題型:選擇題
在密閉的容積可變的容器中通入A、B兩種氣體,在一定條件下反應:2A(g)+B(g)  2C(g) ΔH<0。達到平衡后,改變一個條件,下列量(Y)的變化不符合圖中曲線的是( )
2C(g) ΔH<0。達到平衡后,改變一個條件,下列量(Y)的變化不符合圖中曲線的是( )
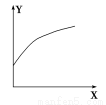
XY
A再加入AB的轉化率
B降低溫度混合氣體的密度
C增大壓強A的轉化率
D升高溫度混合氣體的平均摩爾質量
查看答案和解析>>
科目: 來源:2014年高考化學一輪復習課后規范訓練7-2練習卷(解析版) 題型:選擇題
下列事實不能用勒夏特列原理解釋的是( )
①氯化鐵溶液加熱蒸干最終得不到氯化鐵固體
②鐵在潮濕的空氣中容易生銹
③實驗室可用排飽和食鹽水的方法收集氯氣
④常溫下,將1 mL pH=3的醋酸加水稀釋至100 mL,測得其pH<5
⑤鈉與氯化鉀共融制備鉀:Na(l)+KCl(l)  K(g)+NaCl(l)
K(g)+NaCl(l)
⑥二氧化氮與四氧化二氮的平衡體系,加壓后顏色加深
A.①②③ B.②⑥ C.①③④⑤ D.②⑤⑥
查看答案和解析>>
科目: 來源:2014年高考化學一輪復習課后規范訓練7-2練習卷(解析版) 題型:填空題
已知NO2和N2O4可以相互轉化:2NO2(g)  N2O4(g)(正反應為放熱反應)。現將一定
N2O4(g)(正反應為放熱反應)。現將一定
量NO2和N2O4的混合氣體通入一體積為1 L的恒溫密閉容器中,反應物濃度隨時間變化關系如圖所示,回答下列問題:

(1)圖中共有兩條曲線X和Y,其中曲線________表示NO2濃度隨時間的變化;a、b、c、d四個點中,表示化學反應處于平衡狀態的點是________。
(2)前10 min內用NO2表示的化學反應速率v(NO2)=________mol/(L·min);反應進行至25 min時,曲線發生變化的原因是________。
(3)若要達到與最后相同的化學平衡狀態,在25 min時還可以采取的措施是________。
A.加入催化劑 B.縮小容器體積
C.升高溫度 D.加入一定量的N2O4
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com