
科目: 來源:不詳 題型:單選題
| 物質 | X | Y | Z |
| 初始濃度/mol·L-1 | 0.1 | 0.2 | 0 |
| 平衡濃度/mol·L-1 | 0.05 | 0.05 | 0.1 |
 2Z,其平衡常數為1600
2Z,其平衡常數為1600查看答案和解析>>
科目: 來源:不詳 題型:填空題
 再前推活塞固定在圖乙位置,NO2的轉化率將 (填“增大”、“減小”、或“不變”)。
再前推活塞固定在圖乙位置,NO2的轉化率將 (填“增大”、“減小”、或“不變”)。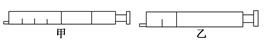
查看答案和解析>>
科目: 來源:不詳 題型:單選題
查看答案和解析>>
科目: 來源:不詳 題型:填空題
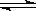 CO2(g)+H2(g)△H<0 試回答下列問題
CO2(g)+H2(g)△H<0 試回答下列問題 :
: 若起始時c(CO)="2" mol·L-1,c(H2O)="3" mol·L-1,達到平衡時CO的轉化率為60%,則在此溫度下,該反應的平衡常數K=
若起始時c(CO)="2" mol·L-1,c(H2O)="3" mol·L-1,達到平衡時CO的轉化率為60%,則在此溫度下,該反應的平衡常數K= 查看答案和解析>>
科目: 來源:不詳 題型:填空題
 2NO2(g)體系中,n(NO)隨時間的變化如表:
2NO2(g)體系中,n(NO)隨時間的變化如表:| 時間(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
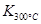 >
>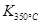 ,則該反應是 熱反應。
,則該反應是 熱反應。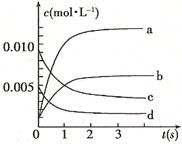
 狀態的是
狀態的是  。
。查看答案和解析>>
科目: 來源:不詳 題型:填空題
查看答案和解析>>
科目: 來源:不詳 題型:單選題
| A.平衡向生成NO2的方向移動 | B.新平衡相對舊平衡,N2O4的轉化率增大 |
| C.N2O4的濃度增大 | D.混合氣體的顏色加深 |
查看答案和解析>>
科目: 來源:不詳 題型:填空題
| 容器代碼 | A | B | C | D |
平衡時 (混) (混) | | | 16 | 17 |
| 平衡時N2轉化率 | 20% | ① | ② | ③ |
| 平衡時H2轉化率 | | 30% | | |
查看答案和解析>>
科目: 來源:不詳 題型:填空題
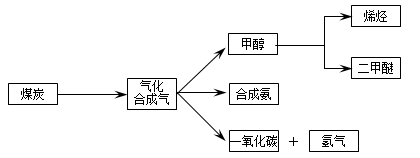
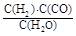 ,它所對應反應的化學方程式為 。
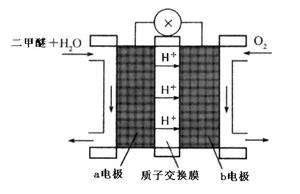
,它所對應反應的化學方程式為 。 溫度230~280℃)進行下列反應:
溫度230~280℃)進行下列反應: CH3OH(g) △H1=-90.7kJ·mol-1
CH3OH(g) △H1=-90.7kJ·mol-1 CH3OCH3(g) +H2O(g) △H2=-23.5kJ·mol-1
CH3OCH3(g) +H2O(g) △H2=-23.5kJ·mol-1 CO2(g)+H2(g) △H3=-41.2kJ·mol-1
CO2(g)+H2(g) △H3=-41.2kJ·mol-1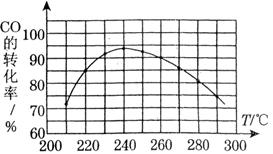
 。
。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com