
 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源:不詳 題型:單選題
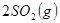
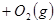

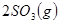 從正方向開始,并達到了平衡,此時
從正方向開始,并達到了平衡,此時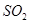 和
和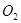 的物質的量之比為2:1,若采取某種措施,導致
的物質的量之比為2:1,若采取某種措施,導致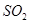 和
和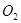 又消耗了一些,并再次達到平衡,下列說法正確的是
又消耗了一些,并再次達到平衡,下列說法正確的是A.新平衡體系中,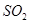 和 和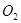 物質的量之比仍為2:1 物質的量之比仍為2:1 |
| B.平衡向正反應方向移動,原因是正反應速率增大,逆反應速率減小 |
C.新平衡體系與舊平衡體系比較,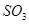 的濃度肯定增大 的濃度肯定增大 |
D.若所采取的措施是縮小容器的容積,則新舊平衡中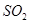 和 和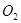 的轉化率之比都是1:1 的轉化率之比都是1:1 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
 pC(g)+ Q在密閉容器中進行,圖中表示在不同反應時間t時,溫度T和壓強P與反應物B在混合氣體中的百分含量B%的關系曲線,由曲線分析下列判斷正確的( )
pC(g)+ Q在密閉容器中進行,圖中表示在不同反應時間t時,溫度T和壓強P與反應物B在混合氣體中的百分含量B%的關系曲線,由曲線分析下列判斷正確的( )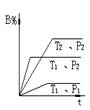
| A.T1 < T2 P1 > P2 m + n >p Q < 0 |
| B.T1 > T2 P1 < P2 m + n >p Q < 0 |
| C.T1 < T2 P1 > P2 m + n <p Q > 0 |
| D.T1 > T2 P1 < P2 m + n <p Q < 0 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
| A.平衡向生成NO2的方向移動 | B.新平衡相對舊平衡,N2O4的轉化率增大 |
| C.N2O4的濃度增大 | D.混合氣體的顏色加深 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
 Z反應影響的示意圖,下列敘述正確的是
Z反應影響的示意圖,下列敘述正確的是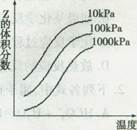
| A.X和Y中只有一種為氣態,z為氣態 |
| B.X、Y、Z均為氣態 |
| C.上述可逆反應的正反應為放熱反應 |
| D.上述反應的逆反應的△H>0 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
 Z(g),經60s達到平衡生成0.3mol的Z,下列說法正確的是( )
Z(g),經60s達到平衡生成0.3mol的Z,下列說法正確的是( )| A.60 s時Z的平衡濃度為O.03mol/L |
| B.將容器容積變為20 L,Z的新平衡濃度將等于原平衡濃度的一半 |
| C.若溫度和體積不變,往容器內增加1 mol Y,Y的轉化率將增大 |
| D.若升高溫度,X的體積分數增大,則正反應的△H>O |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:實驗題
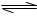 H2(g)+I2(g),體系中n(HI)隨時間變化情況如下表:
H2(g)+I2(g),體系中n(HI)隨時間變化情況如下表:| t/min | 0 | 2 | 4 | 6 | 8 | 10 |
| n(HI)/mol | 0.180 | 0.164 | 0.152 | 0.144 | 0.140 | 0.140 |
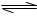 2HI(g)的平衡常數K的值為 。
2HI(g)的平衡常數K的值為 。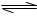 H2(g)+I2(g)的平衡常數,可采取的措施是 (選填字母)。
H2(g)+I2(g)的平衡常數,可采取的措施是 (選填字母)。查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
 WI2(g),當I2的轉化率為20%時,達化學平衡狀態。
WI2(g),當I2的轉化率為20%時,達化學平衡狀態。查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com