
科目: 來源:不詳 題型:單選題
 Fe(s) + H2O,K=0.52。欲使容器中有1.0 mol FeO被還原,反應前容器中應充入a mol H2。則a最接近
Fe(s) + H2O,K=0.52。欲使容器中有1.0 mol FeO被還原,反應前容器中應充入a mol H2。則a最接近| A.1.0 | B.2.0 | C.3.0 | D.4.0 |
查看答案和解析>>
科目: 來源:不詳 題型:單選題
 CH3OH(g) △H<0,下列說法正確的是
CH3OH(g) △H<0,下列說法正確的是| A.一定溫度下,壓縮容器體積,則正反應速率加快,逆反應速率減慢 |
| B.若v生成(CH3OH)=v消耗(CO),則該反應達到平衡狀態 |
C.升高溫度,重新達到平衡時,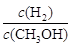 增大 增大 |
| D.使用催化劑,反應的平衡常數增大 |
查看答案和解析>>
科目: 來源:不詳 題型:問答題
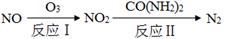
 SO3(g)+NO(g) △H=-41.8 kJ·mol-1
SO3(g)+NO(g) △H=-41.8 kJ·mol-1 2SO3(g) △H=-196.6 kJ·mol-1
2SO3(g) △H=-196.6 kJ·mol-1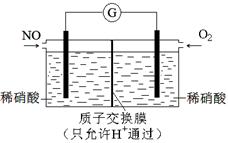
查看答案和解析>>
科目: 來源:不詳 題型:填空題
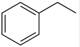 (g)→
(g)→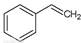 (g)+H2(g),ΔH=" +117.6" kJ/mol
(g)+H2(g),ΔH=" +117.6" kJ/mol| A.因為該反應是吸熱反應,所以升高溫度,正反應速率增大,逆反應速率減小; |
| B.若繼續加入1molCO2、1mol H2,平衡向正反應方向移動; |
| C.若繼續通入1mol CO2則平衡向正反應方向移動,CO2的轉化率增大; |
| D.壓縮體積,平衡不移動,反應物和產物的濃度都不變; |
查看答案和解析>>
科目: 來源:不詳 題型:單選題
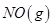 和足量
和足量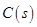 ,發生反應
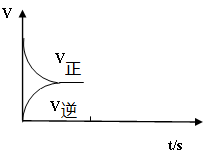
,發生反應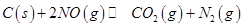 ,平衡狀態時NO(g)的物質的量濃度c(NO)與溫度T的關系如圖所示,則下列說法中,正確的是
,平衡狀態時NO(g)的物質的量濃度c(NO)與溫度T的關系如圖所示,則下列說法中,正確的是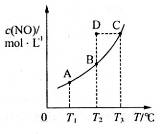
| A.該反應的△H>0 |
B.若該反應在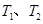 時的平衡常數分別為 時的平衡常數分別為 ,則 ,則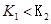 |
C.在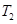 時,若反應體系處于狀態D,則這時一定有 時,若反應體系處于狀態D,則這時一定有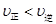 |
D.在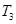 時,若混合氣體的密度不再變化,則可以判斷反應達到平衡狀態 時,若混合氣體的密度不再變化,則可以判斷反應達到平衡狀態 |
查看答案和解析>>
科目: 來源:不詳 題型:單選題
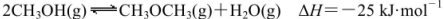 。某溫度下的平衡常數為400。此溫度下,在1L體積不變的密閉容器中加入CH3OH,某時刻測得各組分的物質的量濃度如表,下列說法中不正確的是
。某溫度下的平衡常數為400。此溫度下,在1L體積不變的密閉容器中加入CH3OH,某時刻測得各組分的物質的量濃度如表,下列說法中不正確的是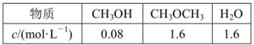
| A.此時刻反應達到平衡狀態 |
| B.容器內壓強不變時,說明反應達平衡狀態 |
| C.平衡時,再加入與起始等量的CH3OH,達新平衡后CH3OH轉化率不變 |
| D.平衡時,反應混合物的總能量降低40 kJ |
查看答案和解析>>
科目: 來源:不詳 題型:填空題
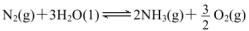
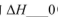 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
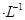 鹽酸與0.2 mol
鹽酸與0.2 mol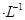 氨水等體積混合,所得混合溶液pH______7(填“>”“<”或“=”,下同),混合溶液中
氨水等體積混合,所得混合溶液pH______7(填“>”“<”或“=”,下同),混合溶液中 (25℃時,NH3.H2O的電離常數
(25℃時,NH3.H2O的電離常數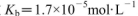 )
)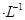 的MgCl2溶液中逐滴加入適量0.lmol
的MgCl2溶液中逐滴加入適量0.lmol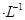 氨水,有白色沉淀生成,向反應后的濁液中,繼續加入O.lmol
氨水,有白色沉淀生成,向反應后的濁液中,繼續加入O.lmol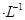 的FeCl3溶液,觀察到的現象是______ ;上述過程中發生的所有反應的離子方程式為______。(25℃時,
的FeCl3溶液,觀察到的現象是______ ;上述過程中發生的所有反應的離子方程式為______。(25℃時,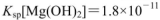 ,
,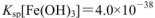 )
)查看答案和解析>>
科目: 來源:不詳 題型:單選題
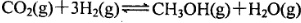 ,5 min后反應達到平衡時c(CH3OH)為0.2 mol
,5 min后反應達到平衡時c(CH3OH)為0.2 mol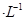 。CO2(g)的平衡物質的量濃度c(CO2)與溫度關系如圖所示。下列說法錯誤的是
。CO2(g)的平衡物質的量濃度c(CO2)與溫度關系如圖所示。下列說法錯誤的是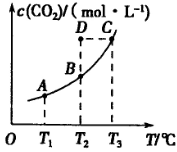
A. 0~5 min,CO2的平均反應速率為0.04 mol.(L.min)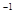 |
B.反應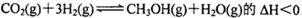 |
C.在T2℃時,若反應處于狀態D,則一定有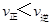 |
| D.若T1℃、T2℃時的平衡常數分別為K1、K2,則K1>K2 |
查看答案和解析>>
科目: 來源:不詳 題型:填空題
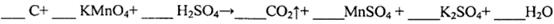
 ,得到如下兩組數據:
,得到如下兩組數據: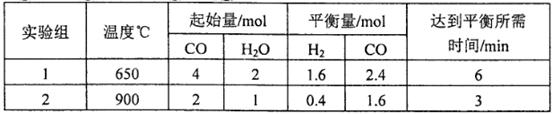
 ____________
____________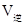 (填“<”,“>”,“=”)。
(填“<”,“>”,“=”)。
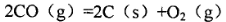
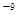 。CaCl2溶液與Na2CO3溶液混合可形成CaCO3沉淀,現將等體積的CaCl2溶液與Na2CO3溶液混合,若Na2CO3溶液的濃度為1×10
。CaCl2溶液與Na2CO3溶液混合可形成CaCO3沉淀,現將等體積的CaCl2溶液與Na2CO3溶液混合,若Na2CO3溶液的濃度為1×10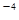 mol/L,則生成沉淀所需CaCl2溶液的最小濃度為__________mol/L。
mol/L,則生成沉淀所需CaCl2溶液的最小濃度為__________mol/L。查看答案和解析>>
科目: 來源:不詳 題型:填空題
| 離子 | K+ | Na+ | NH | SO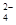 | NO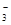 | Cl- |
| 濃度/mol?L-1 | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
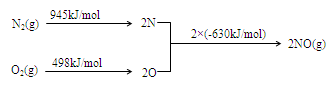
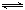 2NO(g)△H= 。
2NO(g)△H= 。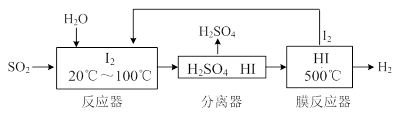
 NiO(OH)+MH,電池放電時,負極電極反應式為 ; 充電完成時,全部轉化為NiO(OH),若繼續充電,將在一個電極產生O2,O2擴散到另一個電極發生電極反應被消耗,從而避免產生的氣體引起電池爆炸。
NiO(OH)+MH,電池放電時,負極電極反應式為 ; 充電完成時,全部轉化為NiO(OH),若繼續充電,將在一個電極產生O2,O2擴散到另一個電極發生電極反應被消耗,從而避免產生的氣體引起電池爆炸。查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com