
科目: 來源:不詳 題型:實驗題
| A.可用過濾的方法除去氫氧化鐵膠體中少量的氯化鐵 |
| B.用酸式滴定管量取18.80mL的碳酸鈉溶液 |
| C.配制0.1mol/L的硫酸時,用量筒量取濃硫酸,要洗滌量筒,否則配制的溶液濃度偏低 |
| D.振蕩用飽和的碳酸鈉溶液吸收乙酸乙酯的試管,發現有氣泡冒出,它是CO2氣體 |
查看答案和解析>>
科目: 來源:不詳 題型:填空題
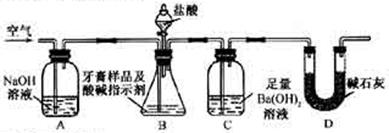
 對某品牌牙膏中摩擦劑成分及其含量進行以下探究:
對某品牌牙膏中摩擦劑成分及其含量進行以下探究: __________________________________________。
__________________________________________。
 ___。
___。 酸鈣的質量分數為__________。
酸鈣的質量分數為__________。查看答案和解析>>
科目: 來源:不詳 題型:實驗題
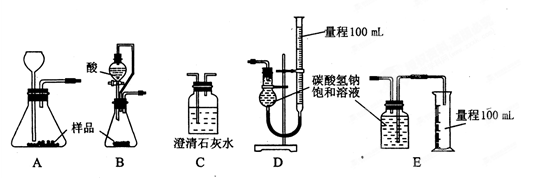
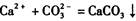 的反應設計了如下方案:稱取樣品→配成溶液→加入足量濃CaCl2溶液→充分反應后過濾→洗滌→干燥→稱量→計算純度。
的反應設計了如下方案:稱取樣品→配成溶液→加入足量濃CaCl2溶液→充分反應后過濾→洗滌→干燥→稱量→計算純度。查看答案和解析>>
科目: 來源:不詳 題型:單選題
| A.堿式滴定管用蒸餾水洗凈后,直接加入未知濃度的NaOH溶液 |
| B.錐形瓶用蒸餾水洗凈后,直接加入一定體積的未知濃度的NaOH溶液 |
| C.滴定前,沒有逐出酸式滴定管尖嘴處的氣泡,滴定終點時氣泡消失 |
| D.滴定前讀數正確,達到滴定終點后,俯視讀數 |
查看答案和解析>>
科目: 來源:不詳 題型:實驗題
| A.純堿 | B.燒堿 | C.膽礬 | D.醋酸鈉 (E) KHSO4 |

查看答案和解析>>
科目: 來源:不詳 題型:填空題

查看答案和解析>>
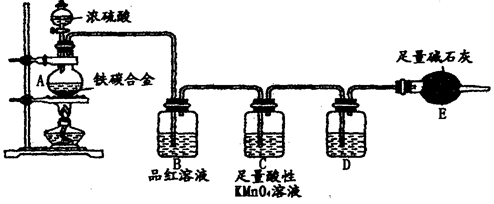
科目: 來源:不詳 題型:實驗題
 5NaC1+NaC1O3+3H2O,今在—5℃的NaOH溶液中通入適量C12(平衡常數K=1.09×1012),此時C12的氧化產物主要是 ;將溶液加熱,溶液中主要離子濃度隨溫度的變化如右圖所示,圖中A、B、C依次表示的離子是 。
5NaC1+NaC1O3+3H2O,今在—5℃的NaOH溶液中通入適量C12(平衡常數K=1.09×1012),此時C12的氧化產物主要是 ;將溶液加熱,溶液中主要離子濃度隨溫度的變化如右圖所示,圖中A、B、C依次表示的離子是 。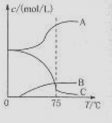
 NaC1O3+3H2↑
NaC1O3+3H2↑ HC1O+H++C1— HC1O
HC1O+H++C1— HC1O H++C1O—
H++C1O—
查看答案和解析>>
科目: 來源:不詳 題型:實驗題
| 滴定 次數 | 待測溶液的體積/mL | 標準溶液的體積 | |
| 滴定前刻度/mL | 滴定后刻度/mL | ||
| 1 | 25.00 | 1.02 | 21.03 |
| 2 | 25.00 | 2.00 | 21.99 |
| 3 | 25.00 | 0.20 | 20.20 |
查看答案和解析>>
科目: 來源:不詳 題型:單選題
| 選項 | 實驗操作、現象 | 解釋、結論 |
| A. | 銅片放入濃硫酸中,無明顯變化 | 銅在冷的濃硫酸中會發生鈍化 |
| B. | 往某氯化物溶液中滴加氨水,產生白色沉淀 | 該氯化物是AlCl3 |
| C. | 將10ml某pH=3的HA溶液加水稀釋到100ml,所得溶液pH=3.8 | HA是弱酸 |
| D. | 往MgCl2溶液中滴加NaOH溶液,調至pH=9時,開始出現沉淀[已知Mg(OH)2的Ksp=5.6×10-12] | 原溶液中 c(Mg2+)=5.6×10-2mol·L-1 |
查看答案和解析>>
科目: 來源:不詳 題型:單選題
| A.分液時,分液漏斗下層液體從下口放出,上層液體從上口倒出 |
| B.提取碘水中的碘單質時,應選擇有機萃取劑,且萃取劑的密度必須比水大 |
| C.用PH試紙測定某無色溶液的PH時,應將PH試紙放入溶液中,觀察其顏色變化,跟標準比色卡比較 |
| D.蒸餾操作中,溫度計應該放在蒸餾燒瓶內的液體中,以測量液體的溫度 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com