
| A、溶液的體積10V甲≥V乙 |
| B、水電離出的OH-濃度:10c(OH-)甲≤c(OH-)乙 |
| C、若分別用等濃度的NaOH溶液完全中和,所得溶液的pH:甲≤乙 |
| D、若分別與5 mL pH=11的NaOH溶液反應,所得溶液的pH:甲≤乙 |
| Kw |
| c(H+) |
| Kw |
| c(H+) |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:
| A、在NaHCO3溶液中:K+、Na+、SO42-、Al3+ |
| B、由水電離的c(H+)=10-12 mol?L-1的溶液:K+、Cu2+、Cl-、Br- |
| C、在pH=1的溶液中:NH4+、K+、NO3-、Cl- |
| D、有NO3-存在的強酸性溶液中:NH4+、Ba2+、Fe2+、Br- |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、標準狀況下,22.4L水的物質的量為1mol |
| B、53g Na2CO3含離子數為0.5NA |
| C、32g甲烷的體積是44.8L |
| D、NA個N2分子的質量為28g |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、向氯化鈣溶液中通入少量CO2,有白色沉淀CaCO3生成 |
| B、向Na2CO3飽和溶液中通入CO2,有NaHCO3結晶析出 |
| C、向NaAlO2溶液中通入過量CO2,有白色膠狀沉淀析出 |
| D、等質量的NaHCO3和Na2CO3分別與足量鹽酸反應,在同溫同壓下生成CO2體積比為53:42 |
查看答案和解析>>
科目:高中化學 來源: 題型:
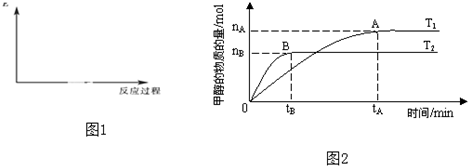
| nA |
| tA |
| C(H2O)?C(CH3OH) |
| C(CO2)?C(H2) |
| nH2 |
| nCH3OH |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com