
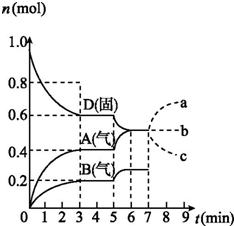
 在容積為2.0 L的密閉容器內,物質D在T℃時發生反應,其反應物和生成物的物質的量隨時間t的變化關系如圖,下列敘述錯誤的是( )
在容積為2.0 L的密閉容器內,物質D在T℃時發生反應,其反應物和生成物的物質的量隨時間t的變化關系如圖,下列敘述錯誤的是( )| A. | 從反應開始到第一次達到平衡時,B物質的平均反應速率為0.033 3 mol/(L•min) | |
| B. | 根據右圖該反應的平衡常數表達式為K=c2(A)•c(B) | |
| C. | 若在第5 min時升高溫度,則該反應的正反應是吸熱反應,反應的平衡常數增大,B的反應速率增大 | |
| D. | 若在第7 分鐘時增加D的物質的量,A的物質的量變化情況符合a曲線 |
分析 A、根據V=$\frac{△c}{△t}$進行計算;
B、根據各物質的增減判斷反應物、生成物,根據同一反應、同一時間段內,各物質的濃度變化量之比等于其計量數之比判斷;化學平衡常數等于平衡時各生成物濃度的化學計量數次冪的乘積除以各反應物濃度的化學計量數次冪的乘積所得的比值;
C、根據溫度升高,D的物質的量減少,A、B的物質的量增大,平衡正向移動,而溫度升高,平衡向吸熱的方向移動;根據平衡常數只有與溫度有關;溫度升高化學反應速率加快;
D、增加固體的物質的量,濃度不變,平衡不移動.
解答 解:A、從反應開始到第一次達到平衡時,A物質的平均反應速率為$\frac{\frac{0.4mol}{2.0L}}{3min}$=0.067mol/L•min,所以v(B)=$\frac{1}{2}$v(A)=0.033 3 mol/(L•min),故A正確;
B、根據圖象知,隨著反應的進行,D的物質的量減少,A、B的物質的量增加,所以D是反應物,A、B是生成物;同一反應、同一時間段內,各物質的濃度變化量之比等于其計量數之比,0-3min時,△D=0.4mol,△A=0.4mol,△B=0.2mol,△D:△A:△B=0.4mol:0.4mol:0.2mol=4:4:2,方程式為:2D(s)?2A(g)+B(g); 因D為固體,所以化學平衡常數K=C2(A)×C(B),故B正確;
C、溫度升高,D的物質的量減少,A、B的物質的量增大,平衡正向移動,而溫度升高,平衡向吸熱的方向移動,說明正反應為吸熱反應,平衡常數只有與溫度有關,溫度升高,平衡正向移動,平衡常數增大;溫度升高化學反應B的反應速率加快,故C正確;
D、D為固體,增加D的物質的量,濃度不變,平衡不移動,A的物質的量變化情況符合b曲線,故D錯誤;
故選D.
點評 本題考查了化學平衡、平衡常數的影響因素,平衡計算分析應用,掌握基礎是關鍵,題目較簡單.


科目:高中化學 來源: 題型:選擇題
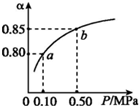 已知2A(g)+B(g)?n C(g),在密閉容器中進行,K(300℃)>K(350℃),某溫度下,A的平衡轉化率(a)與體系總壓強(P)的關系如圖所示.下列說法正確的是( )
已知2A(g)+B(g)?n C(g),在密閉容器中進行,K(300℃)>K(350℃),某溫度下,A的平衡轉化率(a)與體系總壓強(P)的關系如圖所示.下列說法正確的是( )| A. | 該反應正反應是吸熱反應 | |
| B. | 反應溫度升高,A的轉化率增大 | |
| C. | 平衡狀態由a變到b時,化學平衡常數K(A)小于K(B) | |
| D. | 容器內氣體的平均相對分子質量不變,說明反應達到化學平衡狀態 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 X、Y、Z、R、W均為周期表中前四周期的元素,其原子序數依次增大;X2-和Y+有相同的核外電子排布;Z的氫化物的沸點比其上一周期同族元素氫化物的沸點低;R的基態原子在前四周期元素的基態原子中單電子數最多;W為金屬元素,X與W形成的某種化合物與Z的氫化物的濃溶液加熱時反應可用于實驗室制取Z的氣態單質.回答下列問題(相關回答均用元素符號表示):
X、Y、Z、R、W均為周期表中前四周期的元素,其原子序數依次增大;X2-和Y+有相同的核外電子排布;Z的氫化物的沸點比其上一周期同族元素氫化物的沸點低;R的基態原子在前四周期元素的基態原子中單電子數最多;W為金屬元素,X與W形成的某種化合物與Z的氫化物的濃溶液加熱時反應可用于實驗室制取Z的氣態單質.回答下列問題(相關回答均用元素符號表示):查看答案和解析>>
科目:高中化學 來源: 題型:解答題
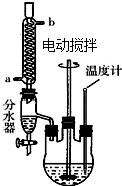 草酸二乙酯可用于苯巴比妥等藥物的中間體,實驗室以草酸(HOOC-COOH)和乙醇為原料制備草酸二乙酯的實驗步驟如下:
草酸二乙酯可用于苯巴比妥等藥物的中間體,實驗室以草酸(HOOC-COOH)和乙醇為原料制備草酸二乙酯的實驗步驟如下: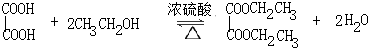 ,
, .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 自然界中的金屬都是以化合態形式存在的 | |
| B. | 工業上可利用反應:Mg+2KCl═MgCl2+2K↑進行金屬鉀的冶煉 | |
| C. | 利用潮汐發電是將化學能轉化為電能 | |
| D. | 將海水蒸干可以直接獲得食用鹽 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 可逆反應就是既能向正反應方向進行,又能向逆反應方向進行的化學反應 | |
| B. | 在催化劑的作用下,二氧化硫與氧氣反應生成三氧化硫的同時,三氧化硫又分解生成二氧化硫和氧氣,因此該反應是可逆反應 | |
| C. | 對于合成氨的反應,如果調控好反應條件,可使一種反應物的轉化率達到100% | |
| D. | 碳酸鈣在高溫下分解生成氧化鈣和二氧化碳,氧化鈣和二氧化碳在常溫下生成碳酸鈣,因此這兩個反應是可逆反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 物質的量濃度相等的CH3COOH和CH3COONa溶液等體積混合:2c(H+)+c(CH3COOH)=c(CH3COO-)+2c(OH-) | |
| B. | 0.1mol/L pH為4的NaHB溶液中:c(HB-)>c(H2B)>c(B2-) | |
| C. | 氯水中:c(Cl-)>c(H+)>c(OH-)>c(ClO-) | |
| D. | pH=3的醋酸溶液與pH=11的氫氧化鈉溶液等體積混合后pH=7 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 4.48L | B. | 5.6L | C. | 6.72L | D. | 8.96L |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | $\frac{c({H}^{+})}{c(O{H}^{-})}$=1×1014的溶液:Ca2+、Na+、ClO-、NO3- | |
| B. | 1.0mol•L-1的KNO3溶液:H+、Fe2+、Cl-、SO42- | |
| C. | 含有0.1mo•L-1的Ca2+溶液:Na+、K+、CO32-、Cl- | |
| D. | 澄清透明的溶液中:Na+、K+、MnO4-、AlO2- |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com