
分析 (1)根據質量比CuSO4:CaO:H2O=1:2:200,計算出CuSO4、CaO質量,再根據n(CuSO4•5H2O)=n(CuSO4),結合m=nM求解CuSO4•5H2O質量,根據n=$\frac{m}{M}$計算CaO的物質的量;
(2)令日均產含Cu量97.5%的粗銅42t需要含雜質23%的精輝銅礦質量為x,根據關系式進行計算,根據硫守恒計算日均產SO2標準狀況下體積;
(3)依據反應:Cu+2FeCl3═CuCl2+2FeCl2、Fe+CuCl2=FeCl2+Cu,4.8g不溶物為銅,根據方程式列出鐵和銅的關系進行求解;
(4)取5.12gCu,物質的量是0.08mol,根據銅元素守恒,Cu最終完全轉化為CuCl2•2H2O晶體,質量是13.68g,完全轉化為 Cu(NO3)2•3H2O晶體,質量是19.36g,反應后溶液有中水54.32g,再經水浴保溫蒸發掉42g,得到的飽和溶液中含有水22.32g,根據溶解度的概念進行計算即可.
解答 解:(1)波爾多液50Kg=50000g,按質量比CuSO4:CaO:H2O=1:2:200配制,m(CuSO4)=50000g×$\frac{1}{1+2+200}$≈246.3g,n(CuSO4)=$\frac{246.3g}{160g/mol}$,n(CuSO4•5H2O)=n(CuSO4)=$\frac{246.3g}{160g/mol}$,m(CuSO4•5H2O)=nM=$\frac{246.3}{160}×250$g≈385g,m(CaO)=50000g×$\frac{2}{1+2+200}$≈492.6g,n(CaO)=$\frac{m}{M}$=$\frac{492.6g}{56g/mol}$≈8.8mol,
故答案為:385;8.8;
(2)設需精輝銅礦的質量為x,根據元素守恒:
Cu2S~~~~~2Cu
160t 128t
x•(1-23%) 42×97.5%t
所以x•77%:42×97.5%t=160t:128t
解得x=66.5t
設日均產SO2標準狀況下體積為y,根據元素守恒:
2Cu~~~~~Cu2S~~~~SO2
128t 1 1
42×97.5%t 1 $\frac{y}{22.4}$
所以42×97.5%t:$\frac{y}{22.4}$=128t:1
解得y=7.17×106,
故答案為:66.5;7.17×106;
(3)將印刷線路板浸入200mL FeCl3溶液中,有11.2g Cu被腐蝕掉,Cu+2FeCl3═CuCl2+2FeCl2、加入Fe粉前,溶液中有Cu2+,Fe2+,Cl-,可能還有Fe3+,向溶液中加入11.2g鐵粉,Fe+CuCl2=FeCl2+Cu,充分反應溶液中還有4.8g不溶物,若無Fe3+,那么Fe恰好把11.2gCu全部置換,不溶物不可能為Fe只能是Cu,則溶解的銅的物質的量為$\frac{11.2g-4.8g}{64g/mol}$=0.1mol,Cu+2FeCl3═CuCl2+2FeCl2、參加反應的FeCl3物質的量為0.2mol,11.2gFe的物質的量為:$\frac{11.2g}{56g/mol}$=0.2mol,Fe+2FeCl3═3FeCl2、參加反應的FeCl3物質的量為0.4mol,
所以原FeCl3溶液的物質的量濃度$\frac{0.2mol+0.4mol}{0.2L}$=3mol/L,
答:原FeCl3溶液的物質的量濃度為3mol/L;
(4)物質混合后發生反應的表達式為:Cu+NO3-+H+=Cu2++H2O+NOx↑,根據20℃溶解度:CuCl2•2H2O 73g/100gH2O,Cu(NO3)2•3H2O,125g/100gH2O,所以Cu(NO3)2•3H2O得溶解度大,硝酸根離子的剩余量很小,所以析出的是CuCl2晶體,取5.12gCu,物質的量是$\frac{5.12g}{64g/mol}$=0.08mol,根據銅元素守恒,生成的氯化銅質量是5.12×$\frac{135}{64}$=10.8g,反應后溶液有水54.32g,再經水浴保溫蒸發掉42g,得到的飽和溶液中含有水12.32g,設析出的晶體中含有氯化銅的質量是S,則$\frac{73×\frac{135}{171}}{100+73×\frac{136}{171}}$=$\frac{S}{100g}$,得S=50g,設最終得到的晶體的化學式為:CuCl2•xH2O,所以$\frac{10.8-8.12×\frac{135}{135+18x}}{12.32-8.12×\frac{18x}{135+18x}}$=$\frac{50.0}{100}$,解得x=3,所以析出的是CuCl2•3H2O.
答:晶體的化學式為:CuCl2•3H2O.
點評 本題考查化學方程式的相關計算,屬于綜合計算題目,注意從元素守恒的角度書寫關系式計算,題目難度較大.


 ABC考王全優卷系列答案
ABC考王全優卷系列答案科目:高中化學 來源: 題型:選擇題
| A. | 化學實驗室不必備有滅火器等防火器材 | |
| B. | 稀釋濃硫酸時要把濃硫酸慢慢注入水中且不斷攪拌 | |
| C. | 化學實驗室空間較小,易燃易爆物跟其他物質可混存 | |
| D. | 一切能產生有毒氣體的實驗均不能在實驗室中進行 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
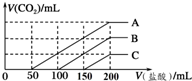 濃度相同的NaOH溶液各100mL倒入A、B、C三個燒杯中,分別向三份溶液中通入不等量的CO2,充分反應后,再向三份所得溶液中逐滴加入0.2mol/L的鹽酸,產生CO2的體積(標準狀況下)與所加鹽酸體積之間關系如圖所示.下列判斷正確的是( )
濃度相同的NaOH溶液各100mL倒入A、B、C三個燒杯中,分別向三份溶液中通入不等量的CO2,充分反應后,再向三份所得溶液中逐滴加入0.2mol/L的鹽酸,產生CO2的體積(標準狀況下)與所加鹽酸體積之間關系如圖所示.下列判斷正確的是( )| A. | 通入CO2后,A燒杯中的溶質成分是Na2CO3 | |
| B. | B燒杯中通入的CO2體積為448 mL | |
| C. | 原NaOH溶液的濃度為0.2 mol/L | |
| D. | 通入CO2后,C燒杯中溶質成分的物質的量之比為n(NaOH):n(Na2CO3)=1:2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 2NO2?N2O4 | B. | 2NO2?2NO+O2 | ||
| C. | 2HI?H2+I2 | D. | FeCl3+3KSCN?Fe(SCN)3+3KCl |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 在某容積一定的密閉容器中,有下列的可逆反應:(g)+B(g)?xC(g)(正反應放熱)有圖Ⅰ所示的反應曲線,試判斷對圖Ⅱ的說法中正確的是(T表示溫度,P表示壓強,C%表示C的體積分數)( )
在某容積一定的密閉容器中,有下列的可逆反應:(g)+B(g)?xC(g)(正反應放熱)有圖Ⅰ所示的反應曲線,試判斷對圖Ⅱ的說法中正確的是(T表示溫度,P表示壓強,C%表示C的體積分數)( )| A. | P3>P4,y軸表示A的物質的量 | |
| B. | P3<P4,y軸表示B的體積分數 | |
| C. | P3<P4,y軸表示混合氣體的密度 | |
| D. | P3>P4,y軸表示混合氣體的平均相對分子質量 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ②>①>③ | B. | ①>②>③ | C. | ③>①>② | D. | ①═②═③ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 弱酸 | HA | HB | H2C |
| 電離平衡常數 (25℃) | K1=1.77×10-4 | K1=4.9×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
| A. | B-+HA→HB+A- | |
| B. | 2Bˉ+H2C→2HB+C2- | |
| C. | 中和等體積、等pH的HA和HB消耗NaOH的量前者小于后者 | |
| D. | 等體積、等濃度的NaA和NaB溶液中所含離子總數前者大于后者 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Na+、Ba2+、NO3-、SO42- | B. | Cl-、K+、H+、SO42- | ||
| C. | Na+、Cl-、K+、Ag+ | D. | Fe2+、SO42-、OH-、Na+ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 甲法多 | B. | 乙法多 | C. | 一樣多 | D. | 無法比較 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com