
| A. | 至少存在4種離子 | |
| B. | Cl-一定存在,且c(Cl )≥0.4 mol/L | |
| C. | SO42-、NH4+,一定存在,Cl-可能不存在 | |
| D. | CO32-、Al3+一定不存在,K+可能存在 |
分析 加入過量NaOH溶液,加熱,得到0.02mol氣體,可知一定存在銨離子;紅褐色沉淀是氫氧化鐵,1.6g固體為三氧化二鐵,可知一定有Fe2+,一定沒有CO32-;
4.66g不溶于鹽酸的沉淀,硫酸鋇沉淀,物質的量為:0.02mol;根據(jù)以上數(shù)據(jù)推算存在離子,根據(jù)電荷守恒推算氯離子的存在及數(shù)據(jù).
解答 解:由于加入過量NaOH溶液,加熱,得到0.02mol氣體,說明一定有NH4+,且物質的量為0.02mol;同時產(chǎn)生紅褐色沉淀,說明一定有Fe2+,1.6g固體為氧化鐵,物質的量為0.01mol,根據(jù)Fe元素守恒,故有0.02molFe2+,一定沒有CO32-;
4.66g不溶于鹽酸的沉淀為硫酸鋇,一定有SO42-,物質的量為0.02mol;根據(jù)電荷守恒,一定有Cl-,至少 0.02mol×3+0.02-0.02mol×2=0.04mol,物質的量濃度至少 $\frac{0.04mol}{0.1L}$=0.4mol/L,
A、至少存在Cl-、SO42-、NH4+、Fe3+四種離子,故A正確;
B、根據(jù)電荷守恒,至少存在0.04molCl-,即c(Cl-)≥0.4mol/L,故B正確;
C、一定存在氯離子,故C錯誤;
D、Al3+無法判斷是否存在,故D錯誤;
故選AB.
點評 本題考查離子共存知識,做題是認真閱讀、分析題中數(shù)據(jù),合理分析,特別是氯離子的推斷,難度中等.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 用濃硫酸與蛋白質的顏色反應鑒別部分蛋白質 | |
| B. | 用乙醇從碘水中萃取碘 | |
| C. | 用乙醇和濃硫酸除去乙酸乙酯中的少量乙酸 | |
| D. | 用食醋浸泡有水垢的水壺清除其中的水垢 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 操作及現(xiàn)象 | 結論 | |
| A | 向AgCl懸濁液中加入NaI溶液時出現(xiàn)黃色沉淀 | Ksp(AgCl)<Ksp(AgI) |
| B | 向某溶液中滴加氯水后再加入KSCN溶液,溶液呈紅色 | 溶液中一定含有Fe2+ |
| C | 向NaBr溶液中滴入少量氯水和苯,振蕩、靜置,溶液上層呈橙紅色 | Br-還原性強于Cl- |
| D | 向溶液X的稀溶液中滴加NaOH稀溶液,將濕潤的紅色石蕊試紙置于試管口,試紙不變藍 | 溶液X中無NH4+ |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 0.1(b-2a)mol•L-1 | B. | 10(2a-b)mol•L-1 | C. | 10(b-a)mol•L-1 | D. | 10(b-2a)mol•L -1 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 選項 | 實驗操作 | 實驗現(xiàn)象 | 結論 |
| A | 用激光筆照射雞蛋白水溶液 | 有丁達爾效應 | 雞蛋白分子直徑介于1nm~100nm |
| B | 向某氯化亞鐵溶液中加入Na2O2粉末 | 出現(xiàn)紅褐色沉淀 | 說明原氯化亞鐵已氧化變質 |
| C | 碳酸鹽X加熱分解,產(chǎn)生的氣體通入酸化的BaCl2溶液 | 產(chǎn)生白色沉淀 | X可能是NaHCO3 |
| D | 濕潤的KI淀粉試紙靠近氣體Y | 試紙變藍 | Y一定是Cl2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1mol醋酸的質量與NA個醋酸分子的質量相等 | |
| B. | NA個氧氣分子和NA個氫氣分子的質量比等于16:1 | |
| C. | 30g乙烷(C2H6)所含的原子數(shù)目為NA | |
| D. | 在標準狀況下,0.5NA個氯氣分子所占體積約是11.2L |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
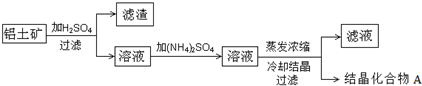
| 實驗 | 實驗步驟 | 實驗結果 |
| ① | 稱取9.06g的結晶化合物A加熱 | 加熱到質量恒定時,質量減輕了4.32g; |
| ② | 將加熱后所得的固體分成兩等份,分別加適量的水,制成溶液. | |
| ③ | 在一份溶液中加入足量的BaCl2溶液. | 產(chǎn)生4.66g 白色沉淀; |
| ④ | 在另一份溶液中,逐滴加入2mol•L-1的NaOH溶液. | 先觀察到產(chǎn)生白色沉淀,接著產(chǎn)生有刺激性氣味的氣體B,沉淀逐漸溶解,當加入25mL的氫氧化鈉溶液時,沉淀恰好完全溶解. |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com