
| 已知 | 類推 | |
| A | 將Fe加入CuSO4溶液中: Fe+Cu2+═Cu+Fe2+ | 將Na加入到CuSO4溶液中: 2Na+Cu2+═Cu+2Na+ |
| B | 向稀硫酸溶液中加入NaOH溶液至中性:H++OH-═H2O | 向稀H2SO4溶液中加入Ba(OH)2溶液至中性:H++OH-═H2O |
| C | 向有水垢的瓶膽內加入足量稀鹽酸溶液: CaCO3+2H+═Ca2++CO2↑+H2O | 向有水垢的瓶膽內加入足量醋酸溶液: CaCO3+2H+═Ca2++CO2↑+H2O |
| D | 向Ca(OH)2溶液中通入過量CO2: CO2+OH-═HCO3- | 向Ca(OH)2溶液中通入過量SO2: SO2+OH-═HSO3- |
| A. | A | B. | B | C. | C | D. | D |
分析 A.金屬鐵可以將金屬銅從其鹽中置換出來,但是活潑金屬鈉和鹽的反應一定是和鹽中的水反應;
B.硫酸和氫氧化鋇反應生成水和硫酸鋇沉淀;
C.稀鹽酸為強酸,醋酸為弱酸,醋酸在離子方程式中需要保留分子式;
D.二氧化碳和二氧化硫均能使澄清的石灰水變渾濁.
解答 解:A.鐵排在金屬銅的前面,金屬鐵可以將金屬銅從其鹽中置換出來,但是活潑金屬鈉和鹽的反應是先和鹽中的水反應,不會置換出其中的金屬,反應的離子方程式為:2Na+2H2O+Cu2+═2Na++Cu(OH)2↓+H2↑,兩個反應不能類推,故A錯誤;
B.硫酸和氫氧化鋇反應生成水和硫酸鋇沉淀,離子反應方程式為:Ba2++2H++2OH-+SO42-=2H2O+BaSO4↓,稀硫酸與NaOH溶液的離子方程式為:H++OH-=H2O,兩個反應的離子方程式不同,不能類推,故B錯誤;
C.水垢的主要成分為碳酸鈣,碳酸鈣與醋酸的離子方程式為:CaCO3+2CH3COOH=Ca2++H2O+CO2↑+2CH3COO-、與鹽酸的離子方程式為:CaCO3+2H+=Ca2++H2O+CO2↑,兩個反應的離子方程式不同,不能類推,故C錯誤;
D.二氧化碳和二氧化硫均能使澄清的石灰水變渾濁,如果氣體過量會變澄清,碳酸鈣和亞硫酸鈣均是難溶于水的鹽,碳酸氫鈣和亞硫酸氫鈣是易溶于水的,可以類推,故D正確;
故選D.
點評 本題考查了離子方程式的書寫判斷,為高考的高頻題,屬于中等難度的試題,注意掌握離子方程式的書寫原則,明確離子方程式正誤判斷常用方法,本題中明確反應實質為解答關鍵.


科目:高中化學 來源: 題型:選擇題
| A. | 分子式和結構都相同,性質可能相同 | |
| B. | 分子式相同,結構不同,化學性質一定不相同 | |
| C. | 相對分子質量一定相同、官能團一定不同 | |
| D. | 相對分子質量和各元素質量分數一定相同,化學性質不一定相同 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 8個中子的碳原子的核素符號:14C | B. | HF的電子式: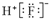 | ||
| C. | Cl-離子的結構示意圖: | D. | 氧化鋁的化學式:AlO |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 元素編號 | 元素性質或原子結構 |
| T | M層的電子數為K層電子數的3倍 |
| X | 其氫化物的空間構型為正四面體 |
| Y | 常溫下單質為雙原子分子,其氫化物水溶液呈堿性 |
| Z | 元素最高正價是+7價 |
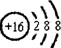 ;元素X的最高價氧化物的電子式
;元素X的最高價氧化物的電子式
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
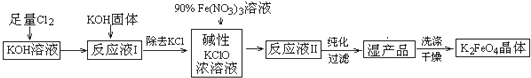
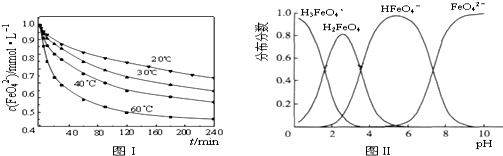
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 元素及其化合物的學習和應用是中學化學的主要任務之一.
元素及其化合物的學習和應用是中學化學的主要任務之一.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
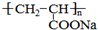 )是一種強吸水樹脂.由某烴A合成聚丙烯酸鈉的流程如圖:
)是一種強吸水樹脂.由某烴A合成聚丙烯酸鈉的流程如圖: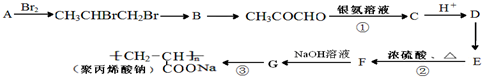
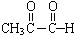 +2Ag(NH3)2OH$\stackrel{△}{→}$
+2Ag(NH3)2OH$\stackrel{△}{→}$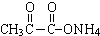 +3NH3+2Ag↓+H2O.
+3NH3+2Ag↓+H2O.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 分子總數為NA的NO2和CO2的混合氣體中含有的氧原子數是2NA | |
| B. | 28g乙烯和環丁烷(C4H8)的混合氣體中含有的碳原子數為2NA | |
| C. | 常溫常壓下,92g的NO2和N2O4混合氣體含有的原子數為6NA | |
| D. | 常溫常壓下,22.4L氯氣與足量鎂粉充分反應后,轉移的電子數為2NA |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
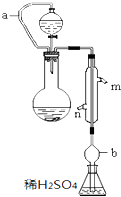 實驗小組測定某肥料中的總氮含量(以氮的質量分數表示),實驗裝置如圖(圖中加熱及夾持儀器略去).稱取1.200g樣品,通過化學方法將肥料中的氮轉化成銨鹽(除樣品外,所加試劑均不含氮元素),然后在堿性溶液中蒸餾氨,用25.00mL濃度為0.5000mol•L-1硫酸溶液充分吸收,再用濃度為0.1000mol•L-1氫氧化鈉溶液滴定未反應的硫酸.重復上述實驗三次.實驗數據如下:
實驗小組測定某肥料中的總氮含量(以氮的質量分數表示),實驗裝置如圖(圖中加熱及夾持儀器略去).稱取1.200g樣品,通過化學方法將肥料中的氮轉化成銨鹽(除樣品外,所加試劑均不含氮元素),然后在堿性溶液中蒸餾氨,用25.00mL濃度為0.5000mol•L-1硫酸溶液充分吸收,再用濃度為0.1000mol•L-1氫氧化鈉溶液滴定未反應的硫酸.重復上述實驗三次.實驗數據如下:| 實驗 次數 | 氫氧化鈉溶液的體積 | |
| 滴定前刻度(mL) | 滴定后刻度(mL) | |
| 1 | 0.00 | 5.22 |
| 2 | 6.00 | 11.18 |
| 3 | 12.00 | 17.20 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com