
【題目】原電池原理應用廣泛。
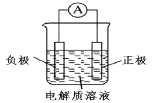
(1)利用原電池裝置可以驗證Fe3+與Cu2+氧化性相對強弱。
如圖所示,該方案的實驗原理是自發(fā)進行的氧化還原反應可以設計為原電池。寫出該氧化還原反應的離子方程式:__________________________,裝置中的負極材料是______(填化學式),正極反應式是_________________________。
(2)某研究性學習小組為證明2Fe3++2I-![]() 2Fe2++I2為可逆反應,設計如下方案:組裝如圖原電池裝置,接通靈敏電流計,指針向右偏轉(注:此靈敏電流計指針是偏向電源正極),隨著時間進行電流計讀數逐漸變小,最后讀數變?yōu)榱恪.斨羔樧x數變零后,在右管中加入1mol/LFeCl2溶液。
2Fe2++I2為可逆反應,設計如下方案:組裝如圖原電池裝置,接通靈敏電流計,指針向右偏轉(注:此靈敏電流計指針是偏向電源正極),隨著時間進行電流計讀數逐漸變小,最后讀數變?yōu)榱恪.斨羔樧x數變零后,在右管中加入1mol/LFeCl2溶液。
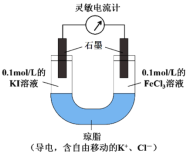
①實驗中,“讀數變?yōu)榱?/span>”是因為___________________。
②“在右管中加入1mol/LFeCl2溶液”后,觀察到靈敏電流計的指針_________偏轉(填“向左”、“向右”或“不”),可證明該反應為可逆反應。
【答案】Cu+2Fe3+=Cu2++2Fe2+ Cu Fe3++e-=Fe2+ 該可逆反應達到了化學平衡狀態(tài) 向左
【解析】
(1)利用原電池裝置可以驗證Fe3+與Cu2+氧化性相對強弱,則發(fā)生的反應為Fe3+生成Cu2+的氧化還原反應,所以負極材料應為Cu,電解質應為含有Fe3+的可溶性鹽溶液。
(2)①實驗中,“讀數變?yōu)榱?/span>”,表明原電池反應已“停止”,即反應達平衡狀態(tài)。
②“在右管中加入1mol/LFeCl2溶液”后,增大了生成物濃度,平衡逆向移動,觀察到靈敏電流計的指針偏轉與原來相反。
(1)利用原電池裝置可以驗證Fe3+與Cu2+氧化性相對強弱,則發(fā)生的反應為Fe3+生成Cu2+的氧化還原反應,離子方程式為Cu+2Fe3+=Cu2++2Fe2+,所以負極材料應為Cu,電解質應為含有Fe3+的可溶性鹽溶液,正極反應式是Fe3++e-=Fe2+。答案為:Cu+2Fe3+=Cu2++2Fe2+;Cu;Fe3++e-=Fe2+;
(2)①實驗中,“讀數變?yōu)榱?/span>”,表明原電池反應已“停止”,即達平衡狀態(tài),由此得出原因為該可逆反應達到了化學平衡狀態(tài)。答案為:該可逆反應達到了化學平衡狀態(tài);
②“在右管中加入1mol/LFeCl2溶液”后,增大了生成物濃度,平衡逆向移動,左邊石墨為正極,右邊石墨為負極,靈敏電流計的指針偏轉與原來相反,即指針向左偏轉。答案為:向左。


科目:高中化學 來源: 題型:
【題目】高鐵酸鉀(K2FeO4)是一種新型、高效、多功能水處理劑,且不會造成二次污染。查閱資料:K2FeO4為紫色固體,微溶于KOH溶液;具有強氧化性,在酸性或中性溶液中快速產生O2,在堿性溶液中較穩(wěn)定。②Cl2與KOH溶液在20 ℃以下反應生成KClO,在較高溫度下則生成 KC1O3。
(1)用K2FeO4處理生活用水既可以消毒又可以沉降,其原理是K2FeO4與水反應生成Fe(OH)3 膠體,寫出該反應的離子方程式:____________________________。
(2)實驗室常利用氯氣制備NaClO后與NaOH、Fe(NO3)3反應制備K2FeO4根據反應原理,僅根據下列儀器,請你組裝合理、簡潔的實驗裝置,所用的裝置的接口連接順序:___________________________。
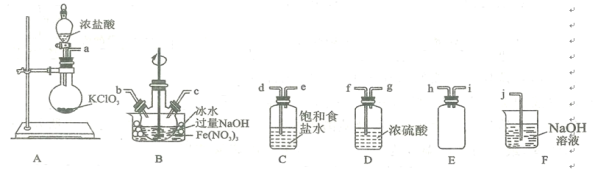
(3)寫出裝置A中發(fā)生的離子方程式: ______________________ 。
(4)三頸燒瓶用冰水浴的原因是 _________________,A處盛放KC1O3的儀器名稱 ___________。
(5)將實驗得到的Na2FeO4再加入飽和KOH溶液中,可析出紫黑色的K2FeO4粗晶體,其原因是________________________________________________________。
(6)高鐵酸鉀純度檢測:稱取3.0 g制備的K2FeO4粗晶體溶于適量KOH溶液中,加入足量的KCrO2充分反應(此時Cr元素全部以CrO42- 形式存在),過濾,濾液在100 mL容量瓶中定容。取10.00 mL加人稀硫酸酸化,再用 0.10 mol/L的(NH4)2Fe(SO4)2標準溶液滴定至終點(此時Cr元素全部以Cr3+形式存在),重復滴定3次,平均消耗(NH4)2Fe(SO4)2溶液的體積為24.00 mL,則該K2FeO4樣品的純度為_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】2015年8月12號接近午夜時分,天津濱海新區(qū)一處集裝箱碼頭發(fā)生爆炸。發(fā)生爆炸的是集裝箱內的易燃易爆物品,爆炸火光震天,并產生巨大蘑菇云。根據掌握的信息分析,裝箱區(qū)的危險化學品可能有鉀、鈉、氯酸鈉、硝酸鉀、燒堿,硫化堿、硅化鈣、三氯乙烯、氯碘酸等。運抵區(qū)的危險化學品可能有環(huán)己胺、二甲基二硫、甲酸、硝酸銨、氰化鈉、4,6-二硝基苯-鄰仲丁基苯酚等。
回答下列問題:
(1)在組成NH4NO3、NaCN兩種物質的元素中第一電離能最大的是__________(填元素符號),解釋原因_____________________________________________
(2)二甲基二硫和甲酸中,在水中溶解度較大的是 (填名稱),原因是_______;燒堿所屬的晶體類型為______;硫化堿(Na2S)的S2-的基態(tài)電子排布式是____________。
(3)硝酸銨中,NO3-的立體構型為 ,中心原子的雜化軌道類型為__________
(4)1mol化合物NaCN中CN-所含的π鍵數為______,與CN-互為等電子體的分子有 。(CN)2又稱為擬鹵素,實驗室可以用氰化鈉、二氧化錳和濃硫酸在加熱條件下制得,寫成該制備的化學方程式___________。
(5)鈉鉀合金屬于金屬晶體,其某種合金的晶胞結構如圖所示。合金的化學式為____________;晶胞中K 原子的配位數為 ;已知金屬原子半徑r(Na)=186pm、r(K)=227pm,計算晶體的空間利用率 ________(列出計算式,不需要計算出結果)。

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知異丁烷的分子結構可簡寫成鍵線式結構為![]() 。有機物X的鍵線式結構為
。有機物X的鍵線式結構為![]() ,有機物Y與等物質的量的H2發(fā)生加成反應可得到有機物X。下列有關說法錯誤的是( )
,有機物Y與等物質的量的H2發(fā)生加成反應可得到有機物X。下列有關說法錯誤的是( )
A. 有機物X的一氯代物只有4種
B. 用系統(tǒng)命名法命名有機物X名稱為2,2,3-三甲基戊烷
C. 有機物X的分子式為C8H18
D. Y的結構可能有3種,其中一種名稱為3,4,4-三甲基-2-戊烯
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在日常生活中,我們經常看到鐵制品生銹、鋁制品表面出現白斑等眾多的金屬腐蝕現象。可以通過下列裝置所示實驗進行探究。下列說法正確的是
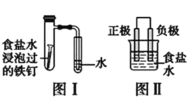
A.按圖Ⅰ裝置實驗,加熱具支試管可更快更清晰地得到實驗證據—觀察到液柱上升
B.圖Ⅱ是圖Ⅰ所示裝置的原理示意圖,圖Ⅱ的正極材料是鐵
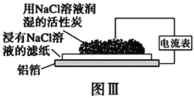
C.鋁制品表面白斑可用圖Ⅲ裝置進行探究,Cl-在鋁箔表面區(qū)發(fā)生電極反應:2Cl- -2e-=Cl2↑
D.圖Ⅲ裝置的總反應為4Al+3O2+6H2O=4Al(OH)3,生成的Al(OH)3脫水形成白斑
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下表各組物質(或者它們的溶液)通過一步反應可實現如圖所示的轉化的是
選項 | X | Y | Z |
|
A | Si | Na2SiO3 | H2SiO3 | |
B | S | H2S | SO2 | |
C | Al2O3 | NaAlO2 | Al2(SO4)3 | |
D | Mg(OH)2 | MgCO3 | MgCl2 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某同學在實驗室中進行如下兩組實驗:①T1K時,將2mL0.02mol·L-1的酸性KMnO4溶液與2mL0.2mol·L-1草酸溶液混合,觀察到溶液完全褪色所需要的時間是4s;②T2K 時,將2mL0.03 mol·L-1的酸性KMnO4溶液與2mL0.2 mol·L-1草酸溶液混合,觀察到溶液完全褪色所需要的時間是5s。下列說法正確的是
A.實驗①反應速率較快B.實驗②反應速率較快
C.無法比較二者反應速率的快慢D.T2—定高于T1
查看答案和解析>>
科目:高中化學 來源: 題型:
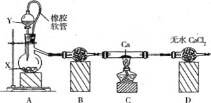
【題目】過氧化鈣主要用作殺菌劑、防腐劑等,溫度在350℃以上容易分解。某同學在實驗室中利用純氧制取少量CaO2,其裝置示意圖如圖:
回答下列問題:
(1)制備氧氣的方法有多種,若X是MnO2,則Y 是____,若Y是H2O,則A中反應的化學方程式為__。
(2)使用橡皮軟管的好處是_____, B中試劑是______.
(3)實驗結束時,該同學取少量C中固體置于水中,發(fā)現有一種刺激性氣味的氣體且該氣體遇石蕊試液變藍色,則該氣體成分是_______。
(4)為測量產品的純度,該同學準確稱量8.00g產品,然后溶解在足量的KI酸性溶液中,充分反應后再取上述溶液總量的一半,用0.2000 mol·L-1Na2S2O3溶液滴定(I2+2Na2S2O3 =2NaI+Na2S4O6,指示劑為淀粉),滴定終點時消耗了VmL標準溶液。判斷滴定 達到終點時的依據是__________,產品中CaO2純度為________%。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在容積為2.00 L的容器中,通入一定量的N2O4,發(fā)生反應N2O4(g)2NO2(g),隨溫度升高,混合氣體的顏色變深。回答下列問題:

(1)反應的ΔH________0(填“大于”或“小于”);100 ℃時,體系中各物質濃度隨時間變化如上圖所示。在0~60 s時段,反應的平衡常數K1為________。
(2)100 ℃時達平衡后,將反應容器的容積增大一倍,平衡向________(填“正反應”或“逆反應”)方向移動,達到新的平衡后N2O4的濃度范圍是___________________
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com