

分析 根據(jù)元素所在周期表中的位置可知a為H元素,b為Na元素,c為Al元素,d為C元素,e為Si元素,f為N元素,g為O元素,h為Cl元素,結(jié)合元素周期律的遞變規(guī)律以及對應物質(zhì)的性質(zhì)進行分析,
(1)g與a可形成化合物a2g為Na2O2,過氧根離子內(nèi)部有非極性鍵,鈉離子與過氧根離子之間有離子鍵;
(2)根據(jù)元素周期律,元素非金屬性越強,氫化物穩(wěn)定性越強;
(3)氧化鋁能與鹽酸反應,而二氧化硅不溶于鹽酸,據(jù)此可以分離提純二氧化硅;
(4)乙烯與水會發(fā)生加成反應生成乙醇;
(5)在氫氧燃料電池中,氫氣是還原劑,氧氣是氧化劑,氫氣與氧氣反應生成水.
解答 解:根據(jù)元素所在周期表中的位置可知a為H元素,b為Na元素,c為Al元素,d為C元素,e為Si元素,f為N元素,g為O元素,h為Cl元素,
(1)g為O元素,a為H元素,g與a可形成化合物a2g為Na2O2,含有的化學鍵類型有離子鍵、非極性鍵,
故答案為:離子鍵、非極性鍵;
(2)e、f、g三種元素氣態(tài)氫化物為:SiH4、NH3、H2O,非金屬性越強,對應的氫化物越穩(wěn)定,非金屬性Si<N<O,故穩(wěn)定性SiH4<NH3<H2O,
故答案為:SiH4<NH3<H2O;
(3)從化合物Al2O3與SiO2組成的混合物中分離提純SiO2,可在混合物中加入鹽酸,再過濾洗滌,
故答案為:H、Cl;
(4)a為H元素,d為C元素,a、d兩種元素可形成多種化合物,其中化合物X的產(chǎn)量是衡量一個國家石油化工發(fā)展水平的標志,X為CH2=CH2,X與H2O在一定條件下反應生成化合物A為乙醇,反應的化學方程式為:CH2=CH2+H2O$\stackrel{一定條件}{→}$CH3CH2OH,
故答案為:CH2=CH2+H2O$\stackrel{一定條件}{→}$CH3CH2OH;
(5)航天技術(shù)中常使用氫氣和氧氣組成的燃料電池,電池反應為2H2+O2═2H2O,故答案為:2H2+O2═2H2O.
點評 本題考查位置結(jié)構(gòu)性質(zhì)的相互關系及應用,題目難度不大,本題關鍵為正確把握元素在周期表中的位置,要求學生熟悉元素周期表.


 100分闖關期末沖刺系列答案
100分闖關期末沖刺系列答案科目:高中化學 來源: 題型:解答題
 煤、天然氣、石油綜合利用是構(gòu)建節(jié)約型、環(huán)境友好型社會的必然選擇.
煤、天然氣、石油綜合利用是構(gòu)建節(jié)約型、環(huán)境友好型社會的必然選擇. .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
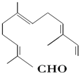 現(xiàn)有試劑:
現(xiàn)有試劑:| A. | ①② | B. | ②③ | C. | ③④ | D. | ①④ |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| 元素代號 | L | M | Q | R | T |
| 原子半徑/nm | 0.160 | 0.143 | 0.089 | 0.102 | 0.074 |
| 主要化合價 | +2 | +3 | +2 | +6、-2 | -2 |
| A. | L2+與R2-的核外電子數(shù)相等 | |
| B. | M與T形成的化合物既能與強酸反應又能與強堿反應 | |
| C. | 氫化物的沸點為H2T>H2R | |
| D. | 單質(zhì)與濃度相等的稀鹽酸反應的劇烈程度為Q>L |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 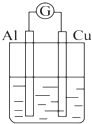 NaOH溶液 | B. | 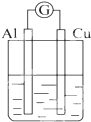 稀硫酸 | C. | 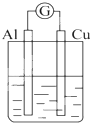 稀硝酸 | D. | 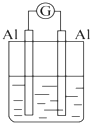 稀鹽酸 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
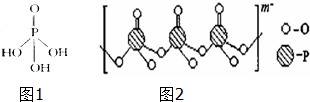 磷單質(zhì)及其化合物在工業(yè)生產(chǎn)巾有著廣泛的應用.向磷可用于制備高純度的磷酸(磷酸結(jié)構(gòu)簡式如圖1),三聚磷酸鈉是常用的水處理劑,次磷酸鈉(NaH2PO2)可用于化學鍍鎳等等.完成下列填空:
磷單質(zhì)及其化合物在工業(yè)生產(chǎn)巾有著廣泛的應用.向磷可用于制備高純度的磷酸(磷酸結(jié)構(gòu)簡式如圖1),三聚磷酸鈉是常用的水處理劑,次磷酸鈉(NaH2PO2)可用于化學鍍鎳等等.完成下列填空:查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ |
 ,該化合物屬于離子(填“共價”或“離子”)化合物.
,該化合物屬于離子(填“共價”或“離子”)化合物. ,該化合物是由極性(填“極性”“非極性”下同)鍵形成的.
,該化合物是由極性(填“極性”“非極性”下同)鍵形成的.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | HCl | B. | CH3Cl | C. | CHCl3 | D. | CCl4 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 ;
;查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權(quán)舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com