
【題目】研究發現,NOx和SO2是霧霾的主要成分。
Ⅰ. NOx主要來源于汽車尾氣,可以利用化學方法將二者轉化為無毒無害的物質。
已知:N2(g)+O2(g) ![]() 2NO(g) ΔH=+180 kJ·mol-1
2NO(g) ΔH=+180 kJ·mol-1
2CO(g)+O2(g) ![]() 2CO2(g) ΔH=-564 kJ·mol-1
2CO2(g) ΔH=-564 kJ·mol-1
(1)2NO(g)+2CO(g)![]() 2CO2(g)+N2(g) ΔH=________.
2CO2(g)+N2(g) ΔH=________.
(2)T℃時,將等物質的量的NO和CO充入容積為2 L的密閉容器中,保持溫度和體積不變,反應過程(0~15 min)中NO的物質的量隨時間變化如圖所示。
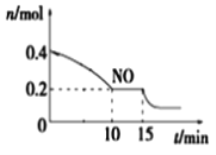
①已知:平衡時氣體的分壓=氣體的體積分數×體系的總壓強,T℃時達到平衡,此時體系的總壓強為p=20MPa,則T℃時該反應的壓力平衡常數Kp =_______;平衡后,若保持溫度不變,再向容器中充入NO和CO2各0.3mol,平衡將_____ (填“向左”、“向右”或“不”)移動。
②15 min時,若改變外界反應條件,導致n(NO)發生如上圖所示的變化,則改變的條件可能是_____(填序號)
A.增大CO濃度 B.升溫 C.減小容器體積 D.加入催化劑
Ⅱ. SO2主要來源于煤的燃燒。燃燒煙氣的脫硫減排是減少大氣中含硫化合物污染的關鍵。
已知:亞硫酸:Ka1=2.0×10-2 Ka2=6.0×10-7
(3)請通過計算證明,NaHSO3溶液顯酸性的原因:_________________________
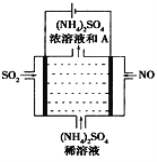
(4)如圖示的電解裝置,可將霧霾中的NO、SO2轉化為硫酸銨,從而實現廢氣的回收再利用。通入NO的電極反應式為____________________;若通入的NO體積為4.48L(標況下),則另外一個電極通入的SO2質量至少為________g。
【答案】 -744 kJ·mol-1 0.0875 (或7/80) 不 AC HSO3-的水解常數K=Kw/Ka1=5.0×10-13<Ka2=6.0×10-7(HSO3-的電離常數),所以顯酸性 6H++ NO+ 5e- = NH![]() +H2O 32
+H2O 32
【解析】
本題考查蓋斯定律、化學平衡常數計算、勒夏特列原理、電離平衡常數、水解平衡常數、水的離子積的關系等。
(1)由蓋斯定律可知:①N2(g)+O2(g) ![]() 2NO(g),②2CO(g)+O2(g)
2NO(g),②2CO(g)+O2(g) ![]() 2CO2(g),②-①得出:△H=(-564-180)kJ·mol-1=-744kJ·mol-1;
2CO2(g),②-①得出:△H=(-564-180)kJ·mol-1=-744kJ·mol-1;
(2) ①2NO(g)+2CO(g)![]() 2CO2(g)+N2(g)
2CO2(g)+N2(g)
起始/mol: 0.4 0.4 0 0
變化/mol: 0.2 0.2 0.2 0.1
平衡/mol: 0.2 0.2 0.2 0.1,
p(NO)=p(CO)=p(CO2)= 20MPa×![]() =
=![]()
p(N2)= 20MPa×![]() =
=![]()
Kp=![]() =
=![]() =0.0875;根據①的分析,化學平衡常數K=5,再向容器中充入NO和CO2各0.3mol,此時的濃度商為仍為5,因此平衡不移動;②15min時,改變某一因素,NO的物質的量減少,說明平衡向正反應方向移動。增大CO的濃度,平衡向正反應方向移動,NO的物質的量減小,A項正確;正反應是放熱反應,升溫,平衡向逆反應方向移動,NO的物質的量增大,B項錯誤;減小容器的體積,相當于增大壓強,平衡向正反應方向移動,NO物質的量減小,C項正確;加入催化劑,化學平衡不移動,D項錯誤;(3)HSO3-的水解常數K=Kw/Ka1=5.0×10-13<Ka2=6.0×10-7,電離平衡常數大于水解
=0.0875;根據①的分析,化學平衡常數K=5,再向容器中充入NO和CO2各0.3mol,此時的濃度商為仍為5,因此平衡不移動;②15min時,改變某一因素,NO的物質的量減少,說明平衡向正反應方向移動。增大CO的濃度,平衡向正反應方向移動,NO的物質的量減小,A項正確;正反應是放熱反應,升溫,平衡向逆反應方向移動,NO的物質的量增大,B項錯誤;減小容器的體積,相當于增大壓強,平衡向正反應方向移動,NO物質的量減小,C項正確;加入催化劑,化學平衡不移動,D項錯誤;(3)HSO3-的水解常數K=Kw/Ka1=5.0×10-13<Ka2=6.0×10-7,電離平衡常數大于水解
平衡常數,說明溶液顯酸性;(4)根據電解裝置,NO和SO2轉化為硫酸銨,說明NO轉化成NH4+,即NO在陰極上發生NO+6H++5e-=NH4++H2O;陽極反應式為SO2+2H2O-2e-=4H++SO42-,根據得失電子數目守恒,因此有2NO~10e-~5SO2,求出SO2的質量為4.48×5×64/(2×22.4)g=32g。


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:
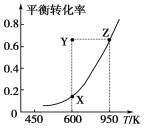
【題目】甲醇脫氫可制取甲醛:CH3OH(g) ![]() HCHO(g)+H2(g)+Q,甲醇的平衡轉化率隨溫度變化曲線如圖所示。下列有關說法正確的是( )
HCHO(g)+H2(g)+Q,甲醇的平衡轉化率隨溫度變化曲線如圖所示。下列有關說法正確的是( )
A. Q>0
B. 600 K時,Y點甲醇的v(正)<v(逆)
C. 從Y點到Z點可通過增大壓強實現
D. 從Y點到X點可通過使用催化劑實現
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】乙炔是重要的化工原料,廣泛用于有機合成和氧炔焊等。生產乙炔的方法有多種,如電石法、甲烷裂解法等。
(1)在Co(NO3)2催化下,乙炔可被50%的濃硝酸(硝酸被還原為NO2)在20~70℃時直接氧化為H2C2O4·2H2O。
①該反應的化學方程式為____________________________________________________;
②實際生產中硝酸可循環利用而不被消耗,用方程式說明:__________________。
(2)電石法原理為:由石油焦與生石灰在電爐中生成電石CaC2(含Ca3P2、CaS等雜質),電石與水反應生成C2H2(含PH3及H2S等雜質)。
①已知焦炭固體與氧化鈣固體每生成l g CaC2固體,同時生成CO氣體吸收7.25kJ的熱量,則該反應的熱化學方程式為______________________________________________;
②用CuSO4溶液凈化乙炔氣體,去除PH3的反應之一為:
4CuSO4+PH3+4H2O==4Cu↓+H3PO4+4H2SO4,每去除1 mol PH3,該反應中轉移電子的物質的量為__________;
③電石法工藝流程簡單、容易操作、乙炔純度高,缺點是___________________(舉1例)。
(3)甲烷裂解法原理為:2CH4(g)![]() C2H2(g)+3H2(g) △H,實驗測得該反應的Kp(用平衡分壓代替濃度計算的平衡常數,分壓=總壓×物質的量分數)與溫度的關系如下圖所示:
C2H2(g)+3H2(g) △H,實驗測得該反應的Kp(用平衡分壓代替濃度計算的平衡常數,分壓=總壓×物質的量分數)與溫度的關系如下圖所示:
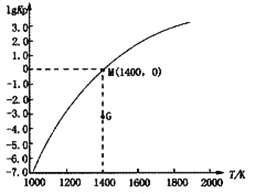
①該反應的△H________0(填“>”、“=”或“<”);
②圖中G點v(正)______v(逆)(填“>”、“=”或“<”);
③M點時,若容器中氣體的總物質的量為1 mol,CH4、C2H2及H2的物質的量分別為a、b、c,則總壓P與a、b、c之間的關系為___________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】25℃下,現有0.1mol·L-1的H2SO4和0.1 mol·L-1一元弱酸HA兩種溶液。
(1)則0.1 mol·L-1一元弱酸HA的電離平衡常數表達式Ka=______________。
(2)0.1mol·L-1的H2SO4中水電離出的C(H+)為____________。
(3)向0.1mol·L-1的硫酸中加入一定體積的pH=13的NaOH溶液,反應后溶液的pH為2,則所需NaOH溶液與硫酸的體積比為_________;
(4)向0.1 mol·L-1一元弱酸HA加入一定體積的水,在此過程中,下列數值變大的是__________。
①c(H+) ② 電離度(α) ③c(OH-) ④ Ka ⑤c(A-)/ c(HA) ⑥n(A-)
(5)實驗室在配制溶液時,一些物質存在水解的情況,在配制Al2(SO4)3溶液時,Al3+也存在水解,請書寫水解離子方程式__________,為了防止Al2(SO4)3發生水解,可加入少量的__________.
(6)已知25 ℃,碳酸的電離平衡常數Ka1= 4.0×10-7,Ka2= 5.6×10-11,則該溫度下NaHCO3的水解平衡常數Kh=_____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】研究人員從木耳菜中提取過氧化物酶(POD),分別與四種不同酚類物質及H2O2進行催化反應,結果如圖所示。下列相關說法正確的是
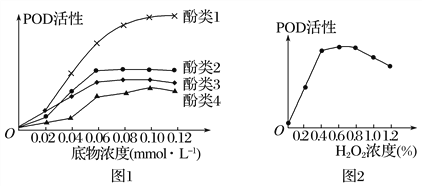
A. 圖1所示的實驗目的是探究不同酚類物質的濃度對POD活性的影響
B. 當底物濃度為0.08 mmolL-1時,POD催化酚類2的反應速率一定大于酚類3
C. 由圖2可知,H2O2濃度過高會抑制POD的活性,降低濃度后POD的活性一定會恢復
D. H2O2對POD活性的影響與溫度和pH對POD活性的影響相同
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將等物質的量的A、B混合于2L的密閉容器中,發生如下反應:3A(g)+B(g)![]() xC(g)+2D(g),經5min后,測得D的濃度為0.5mol/L,C的平均反應速率是0.1mol/(L·min),且此時A的物質的量濃度為0.25 mol/L。
xC(g)+2D(g),經5min后,測得D的濃度為0.5mol/L,C的平均反應速率是0.1mol/(L·min),且此時A的物質的量濃度為0.25 mol/L。
(1)x的值是__________;
(2)B的平均反應速率__________;
(3)則反應開始前放入容器中A的物質的量_____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某反應由兩步反應A→B→C構成,它的反應能量曲線如圖所示(E1、E2、E3、E4表示活化能)。下列有關敘述正確的是( )
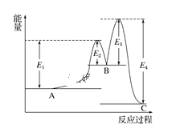
A. 三種化合物中C最穩定B. 加入催化劑會改變反應的焓變
C. 兩步反應均為吸熱反應D. A→C反應中ΔH=E1 - E2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】可逆反應:2NO2![]() 2NO+O2在固定體積的密閉容器中反應,達到平衡狀態的標志是 ( )
2NO+O2在固定體積的密閉容器中反應,達到平衡狀態的標志是 ( )
(1)單位時間內生成n mol O2的同時生成2n mol NO2
(2)單位時間內生成n mol O2的同時,生成2n mol NO
(3)用NO2 、NO、O2的物質的量濃度變化表示的反應速率的比為2:2:2的狀態
(4)混合氣體的顏色不再改變的狀態
(5)混合氣體的平均相對分子質量不再改變的狀態
A. 僅(1)(4)(5) B. 僅(2)(3)(5)
C. 僅(1)(3)(4) D. (1)(2)(3)(4)(5)
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com