
分析 在水溶液里或融融狀態下能導電的化合物是電解質,在水溶液里或熔融狀態下都不能導電的化合物是非電解質,無論是電解質還是非電解質都必須是化合物,據此分析.
解答 解:①金屬鐵是金屬單質,既不是電解質也不是非電解質;
②氯化銨溶于水電離溶液導電屬于電解質;
③硝酸鉀溶液屬于混合物,是電解質溶液,不是電解質;
④單質碘屬于單質,既不是電解質也不是非電解質;
⑤二氧化碳不能電離屬于非電解質;
⑥燒堿 是氫氧化鈉溶于水導電屬于電解質;
⑦硫酸溶于水溶液導電屬于電解質;
⑧氧化鈣熔融導電屬于電解質;
⑨葡萄糖不能電離數非電解質;
⑩食鹽水是氯化鈉的水溶液,不是電解質,
其中屬于電解質的是:②⑥⑦⑧,
屬于非電解質的是⑤⑨,
故答案為:②⑥⑦⑧;⑤⑨.
點評 本題考查了電解質和非電解質的概念,題目難度不大,注意電解質和非電解質的區別.


科目:高中化學 來源: 題型:解答題
 CO2是一種溫室氣體,據科學家預測,到21世紀中葉,全球氣溫將升高1.5-4.5℃,地球氣溫的升高會引起海平面升高,對人類的生存環境產生巨大的影響.如何合理地利用CO2是擺在科學家面前的一個重大課題.回答下列問題:
CO2是一種溫室氣體,據科學家預測,到21世紀中葉,全球氣溫將升高1.5-4.5℃,地球氣溫的升高會引起海平面升高,對人類的生存環境產生巨大的影響.如何合理地利用CO2是擺在科學家面前的一個重大課題.回答下列問題:| CO2的量 | NaOH溶液的量 | 放出的熱量 | |
| ① | 22.0g | 750mL1.0mol•L-1 | xkJ |
| ② | 1.0mol | 2.0mL1.0mol•L-1 | ykJ |
| 物質 | CO2(g) | H2(g) | CH4(g) | H2O(g) |
| 濃度/mol•L-1 | 0.2 | 0.8 | a | 1.6 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 濃硫酸稀釋時應注意將濃硫酸緩緩地倒入盛有水的容量瓶中 | |
| B. | 將11.2L HCl溶于水形成1L溶液,所得溶液的物質的量濃度為0.5mol/L | |
| C. | 0.5mol/L的Na2SO4和1mol/L的NaOH溶液,c(Na+)相同 | |
| D. | 將20g NaOH 溶于1L水中即得到0.5mol/L的NaOH溶液 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①②③④ | B. | ②③④⑤ | C. | ③④⑤⑥ | D. | ④⑤⑥⑦ |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
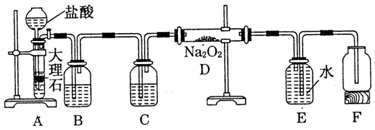
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題

查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 溫度/℃ | 400 | 500 | 800 |
| 平衡常數Kc | 9.94 | 9 | 1 |
| A | B | C | D | E | |
| n(CO2) | 3 | 1 | 0 | 1 | 1 |
| n(H2) | 2 | 1 | 0 | 1 | 2 |
| n(CO) | 1 | 2 | 3 | 0.5 | 3 |
| n(H2O) | 5 | 2 | 3 | 2 | 1 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com