
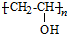 、CH3CH2CH2CHO.
、CH3CH2CH2CHO.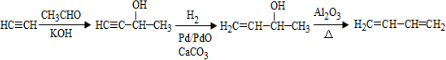 .
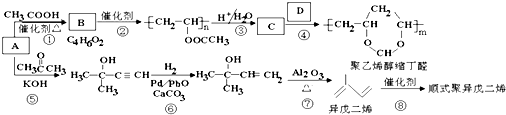
. 分析 由分子式可知A為HC≡CH,由B的分子式、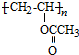 逆推可知B為CH2=CHOOCCH3,結合乙炔(C2H2)和乙酸(C2H4O2)分子式可知B為A與乙酸發生加成反應,B發生加聚反應生成
逆推可知B為CH2=CHOOCCH3,結合乙炔(C2H2)和乙酸(C2H4O2)分子式可知B為A與乙酸發生加成反應,B發生加聚反應生成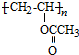 ,水解生成C為
,水解生成C為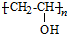 ,由聚乙烯醇縮丁醛可知D為CH3CH2CH2CHO.HC≡CH與丙酮在KOH條件下發生加成反應生成
,由聚乙烯醇縮丁醛可知D為CH3CH2CH2CHO.HC≡CH與丙酮在KOH條件下發生加成反應生成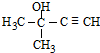 ,與氫氣發生加成反應生成
,與氫氣發生加成反應生成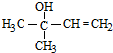 ,在氧化鋁的作用下發生消去反應生成異戊二烯,異戊二烯在催化作用下發生加聚反應生成
,在氧化鋁的作用下發生消去反應生成異戊二烯,異戊二烯在催化作用下發生加聚反應生成 ,以此解答該題.
,以此解答該題.
解答 解:由分子式可知A為HC≡CH,由B的分子式、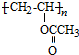 逆推可知B為CH2=CHOOCCH3,結合乙炔(C2H2)和乙酸(C2H4O2)分子式可知B為A與乙酸發生加成反應,B發生加聚反應生成
逆推可知B為CH2=CHOOCCH3,結合乙炔(C2H2)和乙酸(C2H4O2)分子式可知B為A與乙酸發生加成反應,B發生加聚反應生成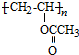 ,水解生成C為
,水解生成C為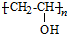 ,由聚乙烯醇縮丁醛可知D為CH3CH2CH2CHO.HC≡CH與丙酮在KOH條件下發生加成反應生成
,由聚乙烯醇縮丁醛可知D為CH3CH2CH2CHO.HC≡CH與丙酮在KOH條件下發生加成反應生成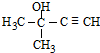 ,與氫氣發生加成反應生成
,與氫氣發生加成反應生成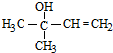 ,在氧化鋁的作用下發生消去反應生成異戊二烯,異戊二烯在催化作用下發生加聚反應生成
,在氧化鋁的作用下發生消去反應生成異戊二烯,異戊二烯在催化作用下發生加聚反應生成 .
.
(1)由以上分析可知A為乙炔,B為CH2=CHOOCCH3,含有的官能團為碳碳雙鍵和酯基,故答案為:乙炔;碳雙鍵和酯基;
(2)A為HC≡CH,與乙酸發生加成反應生成B為CH2=CHOOCCH3,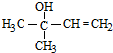 在氧化鋁的作用下發生消去反應生成異戊二烯,
在氧化鋁的作用下發生消去反應生成異戊二烯,
故答案為:加成反應;消去反應;
(3)C為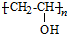 ,D為CH3CH2CH2CHO,故答案為:
,D為CH3CH2CH2CHO,故答案為: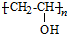 ;CH3CH2CH2CHO;
;CH3CH2CH2CHO;
(4)3-氯-3-甲基-1-丁烯一定條件下發生消去反應生成CH2=C(CH3)-CH=CH2,化學方程式為:CH2=CHC(CH3)2Cl+NaOH$→_{△}^{醇}$CH2=C(CH3)-CH=CH2+NaCl+H2O,
故答案為:CH2=CHC(CH3)2Cl+NaOH$→_{△}^{醇}$CH2=C(CH3)-CH=CH2+NaCl+H2O;
(5)與A具有相同官能團的異戊二烯的所有同分異構體應含有C≡C鍵,可能的結構簡式有CH3CH(CH3)-C≡CH、CH3CH2CH2C≡CH、CH3CH2C≡CCH3等,
故答案為:CH3CH(CH3)-C≡CH、CH3CH2CH2C≡CH、CH3CH2C≡CCH3;
(6)乙炔與乙醛發生加成反應生成HC≡CCHOHCH3,然后與氫氣發生加成反應生成H2C=CHCHOHCH3,在氧化鋁作用下加熱發生消去反應生成CH2=CHCH=CH2,合成路線流程圖為: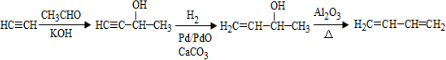 ,
,
故答案為: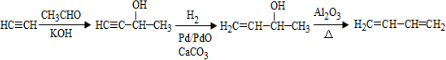 .
.
點評 本題考查有機物推斷與合成,充分利用轉化關系中有機物分子式、結構簡式進行分析,需要學生熟練掌握官能團的性質與轉化,有助于培養學生良好的分析能力和自學能力,難度適中.


科目:高中化學 來源: 題型:解答題
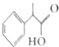 所示.
所示.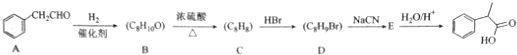
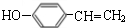 .
.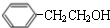 $→_{△}^{濃硫酸}$
$→_{△}^{濃硫酸}$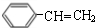 +H2O;C→D的反應類型為加成反應.
+H2O;C→D的反應類型為加成反應.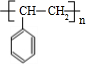 .
. )的敘述正確的是B(填字母序號)
)的敘述正確的是B(填字母序號)查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 1L溶液中含有0.3NA個K+離子 | |
| B. | 1L溶液中含有K+和SO42-離子總數為0.9NA | |
| C. | 2L溶液中含K+的物質的量濃度為1.2mol/L | |
| D. | 2L溶液中含0.6NA個SO42-離子 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 22.4LCH4和CH3Cl的混合物所含有的分子數目為NA | |
| B. | 1mol過氧化氫分子中共用電子對數為3NA | |
| C. | 用惰性電極電解1 L濃度均為2 mol/L的AgNO3與Cu(NO3)2的混合溶液,當有0.2 NA個電子轉移時,陰極析出6.4g金屬 | |
| D. | 0.1mol Na2CO3•10H2O在晶體中或溶液中,含有的CO32-離子均小于0.1 NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
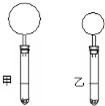 右下圖是10mLpH均為2的鹽酸和醋酸分別與足量的碳酸鈣完全反應后,所觀察到的實驗現象(反應過程中產生的氣體全部收集在試管上部的氣球中).下列說法不正確的是( )
右下圖是10mLpH均為2的鹽酸和醋酸分別與足量的碳酸鈣完全反應后,所觀察到的實驗現象(反應過程中產生的氣體全部收集在試管上部的氣球中).下列說法不正確的是( )| A. | 乙試管中盛放的是鹽酸溶液 | |
| B. | 甲試管中盛放的是醋酸溶液 | |
| C. | 反應開始時的速率:甲>乙 | |
| D. | 反應結束時消耗碳酸鈣的質量:甲>乙 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
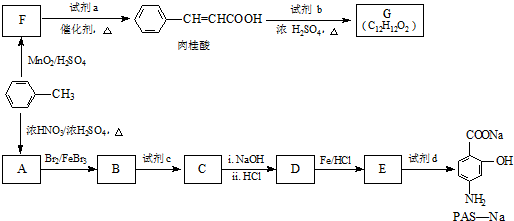
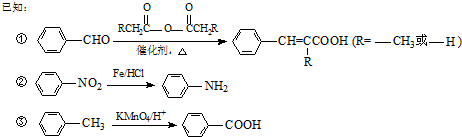
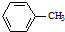 生成A的反應類型是取代反應.
生成A的反應類型是取代反應.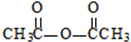 .
.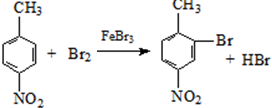 .
.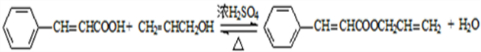 .
. .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 選項 | 實驗操作 | 實驗現象 | 結論 |
| A | 向AgNO3溶液中加入過量氨水 | 由白色沉淀生成 | Ag+與NH3•H2O不能共存 |
| B | 向2ml2%的CuSO4溶液中加入0.5mol/L的NaOH溶液,震蕩后低價幾滴M溶液,加熱 | 未出現磚紅的沉淀 | M不屬于醛類物質 |
| C | 向NaAlO2溶液中滴加飽和NaHCO3溶液 | 由白色沉淀生成 | 驗證兩者都發生了水解反應,且相互促進 |
| D | 向草酸溶液中低價幾滴紫色酸性KmnO4溶液,震蕩 | 溶液紫色褪去 | 草酸具有還原性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com