
| A. | 22.4LCH4和CH3Cl的混合物所含有的分子數目為NA | |
| B. | 1mol過氧化氫分子中共用電子對數為3NA | |
| C. | 用惰性電極電解1 L濃度均為2 mol/L的AgNO3與Cu(NO3)2的混合溶液,當有0.2 NA個電子轉移時,陰極析出6.4g金屬 | |
| D. | 0.1mol Na2CO3•10H2O在晶體中或溶液中,含有的CO32-離子均小于0.1 NA |
分析 A.混合氣體所處的條件不知,則Vm的數值不知,無法計算;
B.過氧化氫的電子式為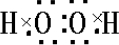 ,由電子式可判斷共用電子對數;
,由電子式可判斷共用電子對數;
C.Ag+氧化性大于Cu2+,根據陽離子的放電順序判斷;
D.在晶體中CO32-不發生水解,在溶液中發生水解.
解答 解:A.Vm受溫度和壓強的影響,溫度和壓強不知,則Vm的數值不知,無法計算物質的量及分子數,故A錯誤;
B.過氧化氫的電子式為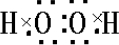 ,由電子式可知,1mol過氧化氫分子中共用電子對數為3NA,故B正確;
,由電子式可知,1mol過氧化氫分子中共用電子對數為3NA,故B正確;
C.Ag+氧化性大于Cu2+,1L濃度均為2mol/L的AgNO3與Cu(NO3)2的混合溶液,當有0.2mol電子轉移時,首先析出Ag,質量為0.2mol×108g/mol=21.6g,故C錯誤;
D.在晶體中CO32-不發生水解,在溶液中發生水解,因此晶體中CO32-離子數為0.1 NA,溶液中CO32-離子小于0.1 NA,故D錯誤;
故選B.
點評 本題考查阿伏伽德羅常數的計算與判斷,題目難度中等,涉及知識點較多、綜合性較強,充分考查學生的分析、理解能力及靈活應用基礎知識的能力,注意放電順序和水解發生的條件.


 口算題天天練系列答案
口算題天天練系列答案科目:高中化學 來源: 題型:解答題
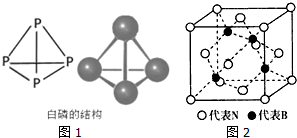 利用周期表中同族元素的相似性,可預測元素的性質.
利用周期表中同族元素的相似性,可預測元素的性質.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
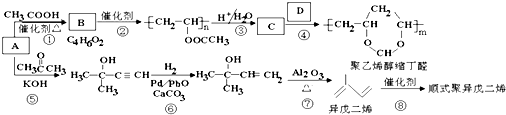
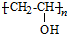 、CH3CH2CH2CHO.
、CH3CH2CH2CHO.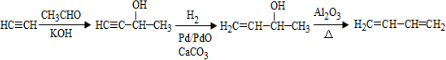 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 新制的氯水在光照下顏色變淺 | |
| B. | 氫氧化鐵膠體加熱生成紅褐色沉淀 | |
| C. | 在合成氨的反應中,降溫或加壓有利于氨的合成 | |
| D. | Fe(SCN)3溶液中加入6mol/L NaOH溶液后顏色變淺 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ②⑥⑦⑧ | B. | ③④⑤⑥ | C. | ③④⑥⑦ | D. | ①②⑧ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Mg和Al | B. | Mg和Zn | C. | Al和Zn | D. | Al和Fe |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
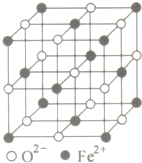 有些食物中鐵元素含量非常豐富,其中非血紅素鐵是其存在的形式之一,主要是三價鐵與蛋白質和羧酸結合成絡合物.
有些食物中鐵元素含量非常豐富,其中非血紅素鐵是其存在的形式之一,主要是三價鐵與蛋白質和羧酸結合成絡合物.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com