
 .
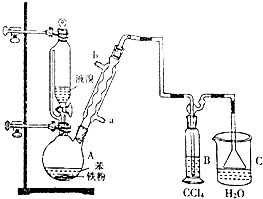
.分析 根據實驗裝置圖可知,在裝置A中用苯與溴在鐵粉作催化劑的條件下生成溴苯和溴化氫,由于苯和液溴都是易揮發的物質,為了提高原料的利用率,用球形冷凝管進行冷凝回流,生成的溴化氫氣體中含有少量的溴蒸,用B裝置中的四氯化碳除去溴化氫中的溴蒸汽,在裝置C中用水吸收生成的溴 化氫,由于溴化氫極易溶于水,所以在用水吸收溴化氫的時候用防倒吸裝置.
(1)A中用苯與溴在鐵粉作催化劑的條件下生成溴苯和溴化氫;
(2)該反應為放熱反應,苯和液溴均易揮發,溴蒸氣是一種紅棕色的氣體,據此分析解答;
(3)采用冷凝管的作用是將揮發出的反應物蒸氣冷凝使其回流到反應容器中;冷凝水的水流方向和氣流方向相反,逆流冷凝效果好,需下口進,上口出;溴極易溶于四氯化碳,
B中盛放的CCl4的作用是除去溴化氫氣體中的溴蒸氣;
(4)根據上面的分析可知,C中是用水吸收的溴化氫,能與硝酸銀溶液反應生成淺黃色沉淀,溴化氫溶液呈酸性能使石蕊試紙變紅;
(5)得到粗溴苯中含有苯、溴、溴化鐵等雜質,要先用水洗除溴化鐵,再用堿洗除溴,再水洗除堿等,再干燥、蒸餾除苯,據此答題.
解答 解:(1)A中用苯與溴在鐵粉作催化劑的條件下反應,苯環上的一個氫原子被一個溴原子取代,其反應方程式為: ,
,
故答案為: ;
;
(2)由于反應放熱,反應液微沸,苯和液溴均易揮發,溴蒸氣是一種紅棕色的氣體,有紅棕色氣體充滿A容器,
故答案為:反應液微沸;有紅棕色氣體充滿A容器;
(3)溴與苯發生取代反應生成溴苯與溴化氫,反應放熱,冷凝管的作用是冷凝揮發出來的苯和液溴,并使它們流回到燒瓶中,冷凝水的水流方向和氣流方向相反,下口進,上口出,所以加熱A前,需先從“a”口通入水,克服水的重力充滿冷凝管,與氣體逆流,冷凝效果好,根據相似相溶原理,溴極易溶于四氯化碳,而溴化氫則不溶,所以C中盛放CCl4的作用是除去溴化氫氣體中的溴蒸氣,
故答案為:冷凝回流;a;除去溴化氫氣體中的溴蒸氣;
(4)證明苯和液溴發生的是取代反應而不是加成反應,即證明有溴化氫產生即可,所以加入硝酸銀溶液后溶液中有淺黃色沉淀產生,或者用藍色石蕊試紙檢驗溴化氫的存在,
故答案為:有淡黃色沉淀生成;藍色石蕊;
(5)得到粗溴苯中含有苯、溴、溴化鐵等雜質,要先用水洗除溴化鐵,再用堿洗除溴,再水洗除堿等,再干燥、蒸餾除苯,所以實驗的正確的操作順序是②④②③①,
故答案為:b.
點評 本題考查有機物實驗制備,涉及溴苯的制取,側重考查學生對裝置與原理的分析評價,明確各個裝置的作用及基本操作方法,題目難度中等.


科目:高中化學 來源: 題型:選擇題
| A. | 乙烯使酸性KMnO4溶液褪色 | |
| B. | 乙烯使溴水褪色 | |
| C. | 點燃乙烯出現黑煙 | |
| D. | 甲烷與氯氣的混合氣體,光照一段時間后褪色 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=-57.3 kJ•mol-1,則含20.0 g NaOH的稀溶液與稀醋酸完全中和,放出的熱量小于28.65kJ | |
| B. | 已知2H2(g)+O2(g)=2H2O(g)△H=-483.6 kJ•mol-1,則標況下1mol氫氣完全燃燒放出241.8 kJ的熱量 | |
| C. | 已知2C(s)+2O2(g)=2CO2(g)△H=a kJ•mol-1,2C(s)+O2(g)=2CO(g)△H=b kJ•mol-1,則a>b | |
| D. | 已知P (白磷,s)=P (紅磷,s)△H<0,則白磷比紅磷穩定 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
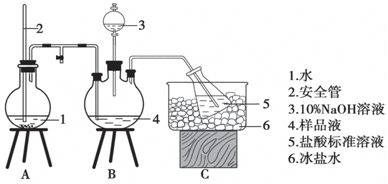 某小組以CoCl2•6H2O、NH4Cl、H2O2、濃氨水為原料,在活性炭催化下,合成了橙黃色晶體X.為確定其組成,進行如下實驗.
某小組以CoCl2•6H2O、NH4Cl、H2O2、濃氨水為原料,在活性炭催化下,合成了橙黃色晶體X.為確定其組成,進行如下實驗.| 銀鹽 性質 | AgCl | AgBr | AgCN | Ag2CrO4 | AgSCN |
| 顏色 | 白 | 淺黃 | 白 | 磚紅 | 白 |
| 溶解度(mol•L-1) | 1.3410-6 | 7.110-7 | 1.110-8 | 6.510-5 | 1.010-6 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
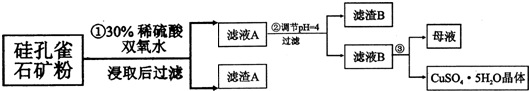
| 氫氧化物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
| 開始沉淀的pH | 3.3 | 1.5 | 6.5 | 4.2 |
| 沉淀完全的pH | 5.2 | 3.7 | 9.7 | 6.7 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com