
| A. |  四種基本反應類型與氧化還原反應的關系 | |
| B. | 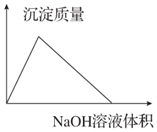 AlCl3溶液中滴加NaOH溶液生成沉淀的情況 | |
| C. |  Ba(OH)2溶液中滴加硝酸溶液導電性的情況 | |
| D. |  等體積等濃度稀硫酸分別與足量鐵和鎂反應的情況 |
分析 A.氧化還原反應的特征為有元素化合價的升降,置換反應一定屬于氧化還原反應,復分解反應一定不屬于氧化還原反應,有單質生成的分解反應屬于氧化還原反應,有單質參加的化合反應屬于氧化還原反應;
B.氯化鋁溶液中加入氫氧化鈉溶液先發生Al3++3OH-═Al(OH)3↓生成沉淀,后發生Al(OH)3+NaOH═NaAlO2+2H2O沉淀溶解至最后消失,結合方程式判斷前后消耗氫氧化鈉溶液體積關系;
C.硝酸和氫氧化鋇的反應方程式為2HNO3+Ba(OH)2=Ba(NO3)2+2H2O,隨著硝酸的加入,溶液體積增大,則離子的濃度逐漸減小,但不可能為0,導電性也也減弱;
D.等體積等濃度稀硫酸分別與足量鐵和鎂反應,生成氫氣的體積相等,Mg與硫酸反應速率較快.
解答 解:A、復分解反應一定不屬于氧化還原反應,則不會出現交叉,置換反應一定屬于氧化還原反應,則應為包含,部分的化合與分解反應屬于氧化還原反應,則不能是包含,應為交叉關系,故A正確;
B.氯化鋁溶液中加入氫氧化鈉溶液先發生Al3++3OH-═Al(OH)3↓生成沉淀,后發生Al(OH)3+NaOH═NaAlO2+2H2O沉淀溶解至最后消失,由方程式可知,前后NaOH溶液體積之比為3:1,故其圖象為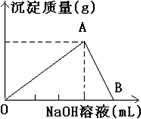 ,故B錯誤;
,故B錯誤;
C.硝酸和氫氧化鋇的反應方程式為2HNO3+Ba(OH)2=Ba(NO3)2+2H2O,隨著硝酸的加入,溶液體積增大,則離子的濃度逐漸減小,但不可能為0,導電性也也減弱,圖象與實際不相符,故C錯誤;
D.等體積等濃度稀硫酸分別與足量鐵和鎂反應,硫酸完全反應,生成氫氣的體積相等,Mg與硫酸反應速率較快,圖象與實際不相符,故D錯誤,
故選A.
點評 本題是圖象解析題,分析圖象時要注意曲線的“原點”、“轉折點”等的意義,對“數據”、“形狀”、“含義”、“性質”進行綜合思考,從中發掘隱含信息快速解題,側重對學生綜合能力的考查.


科目:高中化學 來源: 題型:選擇題
| A. | NaHSO4和Ba(OH)2 | B. | AlCl3和NaOH | C. | NaAlO2和H2SO4 | D. | Na2CO3和HCl |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | H2S?2H++S2- | B. | H2S+H2O?H3O++HS- | ||
| C. | HCl?H++Cl- | D. | HClO═H++ClO- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 氯化亞鐵溶液中加入稀硝酸:3Fe2++4H++NO3-═3Fe3++2H2O+NO↑ | |
| B. | 氧化亞鐵溶于稀硝酸:3Fe2++4H++NO3-═3Fe3++NO↑+3H2O | |
| C. | NH4HCO3溶液與足量Ba(OH)2溶液混合:HCO3-+Ba2++OH-═BaCO3↓+H2O | |
| D. | AlCl3溶液中加入足量的氨水:Al3++4OH-═AlO2-+2H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 上述反應中氧化劑和還原劑的物質的量之比為5:6 | |
| B. | 產生白色煙霧的原因是生成的P2O5白色固體小顆粒(煙)吸水性很強,吸收空氣中的水分,生成酸滴(霧) | |
| C. | 上述反應中消耗3molP時,轉移電子的物質的量為15mol | |
| D. | 產物P2O5為酸性氧化物,但不是磷酸的酸酐 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 電子從Zn極流出,流入Fe極,經鹽橋回到Zn極 | |
| B. | 燒杯b中發生的電極反應為Zn-2e-═Zn2+ | |
| C. | 燒杯a中發生反應O2+4H++4e-═2H2O,溶液pH降低 | |
| D. | 向燒杯a中加入少量KSCN溶液,則溶液會變成紅色 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | NH3$→_{催化劑}^{O_{2}}$NO$\stackrel{NaOH溶液}{→}$NaNO3 | |
| B. | Fe2O3$→_{高溫}^{Al}$Fe$→_{點燃}^{Cl_{2}}$FeCl3 | |
| C. | SiO2$→_{△}^{H_{2}O}$H2SiO3$\stackrel{NaOH溶液}{→}$NaSiO3 | |
| D. | NaSO4溶液$\stackrel{BaCl_{2}溶液}{→}$BaSO4$\stackrel{鹽酸}{→}$BaCl2 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com