
【題目】Ⅰ.尿素[CO(NH2)2]是一種非常重要的高效氮肥,工業上以NH3、CO2為原料生產尿素,該反應實際為兩步反應:
第一步:2NH3(g)+CO2(g)===H2NCOONH4(s) ΔH=-272kJ·mol-1
第二步:H2NCOONH4(s)===CO(NH2)2(s)+H2O(g) ΔH=+138kJ·mol-1
(1)寫出工業上以NH3、CO2為原料合成尿素的熱化學方程式:_________________________
(2)某實驗小組模擬工業上合成尿素的條件,在一體積為0.5 L密閉容器中投入4 mol氨和1mol二氧化碳,實驗測得反應中各組分的物質的量隨時間的變化如下圖所示:
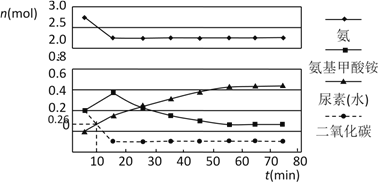
已知總反應的快慢由慢的一步決定,則合成尿素總反應的快慢由第_________步反應決定,總反應進行到_________min時到達平衡。
(3)電解尿素[CO(NH2)2]的堿性溶液制純凈氫氣的過程中同時產生氮氣。電解時,陽極的電極反應式為________________________________。
Ⅱ.用焦炭還原NO2的反應為:2NO2(g)+2C(s )![]() N2(g)+2CO2(g),在恒溫條件下,1 mol NO2和足量C發生該反應,測得平衡時NO2和CO2的物質的量濃度與平衡總壓的關系如圖所示:
N2(g)+2CO2(g),在恒溫條件下,1 mol NO2和足量C發生該反應,測得平衡時NO2和CO2的物質的量濃度與平衡總壓的關系如圖所示:
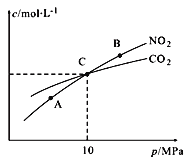
①A、B兩點的濃度平衡常數關系:Kc(A)_______Kc(B) (填 “﹥”、“<”或“﹦”)。
②計算C點時該反應的壓強平衡常數Kp(C)=______(Kp是用平衡分壓代替平衡濃度計算,分壓=總壓×物質的量分數)。
【答案】 2NH3(g)+CO2(g)![]() H2O(g)+CO(NH2)2 (s) ΔH=-134kJ/mol 2 55 CO(NH2)2+8OH--6e-=CO32-+N2↑+6H2O = 2 MPa
H2O(g)+CO(NH2)2 (s) ΔH=-134kJ/mol 2 55 CO(NH2)2+8OH--6e-=CO32-+N2↑+6H2O = 2 MPa
【解析】Ⅰ.(1)已知:①2NH3(g)+CO2(g)═H2NCOONH4(s)△H=-272kJmol-1;②H2NCOONH4(s)═CO(NH2)2(s)+H2O(g)△H=+138kJmol-1;根據蓋斯定律,①+②可得:2NH3(g)+CO2(g)H2O(g)+CO(NH2)2 (s)△H=-134kJ/mol,故答案為:2NH3(g)+CO2(g)H2O(g)+CO(NH2)2 (s)△H=-134kJ/mol;
(2)①由圖象可知在15分鐘左右,氨氣和二氧化碳反應生成氨基甲酸銨后不再變化發生的是第一步反應,氨基甲酸銨先增大再減小最后達到平衡,發生的是第二步反應,從曲線斜率不難看出第2步反應速率慢,所以合成尿素總反應的快慢由第2步反應決定,根據圖可知,尿素在55分鐘時,物質的量不再變化,即反應達到平衡,所以總反應進行到55min時到達平衡,故答案為:2;55;
(3)電解尿素[CO(NH2)2]的堿性溶液制純凈氫氣的過程中同時產生氮氣,電解時,陽極上發生氧化反應得到氧化產物,即為氮氣,電極反應式為CO(NH2)2+8OH--6e-=CO32-+N2↑+6H2O,故答案為:CO(NH2)2+8OH--6e-=CO32-+N2↑+6H2O;
Ⅱ.①A、B兩點的溫度相同,平衡常數K只與溫度有關,故濃度平衡常數關系:Kc(A)=Kc(B);故答案為:=;
②1molNO2和足量C發生該反應,設反應二氧化氮x,列三段式:
2NO2(g)+2C(s) ![]() N2(g)+2CO2(g)
N2(g)+2CO2(g)
n始: 1 0 0
n轉: x 0.5x x
n平: 1-x 0.5x x
從圖知C點時NO2和CO2的物質的量濃度,則1-x=x,解得x=0.5,則平衡時總的物質的量為1.25mol,C點時該反應的壓強平衡常數Kp(C)= 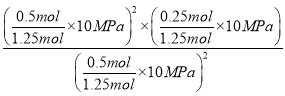 =2MPa;故答案為:2MPa。
=2MPa;故答案為:2MPa。


 備戰中考寒假系列答案
備戰中考寒假系列答案科目:高中化學 來源: 題型:
【題目】下列化學反應中,屬于氧化還原反應的是
A. SO3+H2O=H2SO4 B. CaCO3![]() CaO+CO2↑
CaO+CO2↑
C. Zn+H2SO4=ZnSO4+H2↑ D. AgNO3+HCl=AgCl↓+HNO3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知:25℃時H2C2O4的pKa1=1.22,pK a2=4.19,CH3COOH的pK a=4.76(電離常數K的負對數-1gK=pK)。下列說法正確的是
A. 濃度均為0.1mol·L-1NH4HC2O4和CH3COONH4溶液中:c(NH4+)前者小于后者
B. 0.1 mol·L-1KHC2 O 4溶液滴加氨水至中性:(NH4+)<c(C2O42-)
C. 0.1 mol·L-1K2C2O4溶液滴加鹽酸至pH=1.22:C(H+)-c(OH-)=c(Cl-)-3c(HC2O4-)
D. 0.1 mol·L-1CH3COONa溶液中滴加KHC2O4溶液至PH=4.76;c(K+)>c(Na+)>c(HC2O4-)>c(C2O42-)>c(CH3COO-)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某溶液中含有Ba2+、Cu2+、Ag+,現用NaOH溶液、鹽酸和Na2SO4溶液將這三種離子逐一沉淀分離。其流程如下圖,已知沉淀2為藍色。
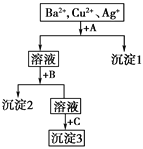
(1)寫出沉淀的化學式:沉淀1______;沉淀3________。
(2)寫出混合液+A的離子方程式_________________,溶液+B的離子方程式________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】生物柴油是一種用植物油、動物油或廢棄油脂等為原料加工而成的清潔燃料,主要成分為高級脂肪酸甲酯。一種用菜籽油等為原料制備生物柴油的實驗步驟如下:
①向右圖所示的三口燒瓶中加入3.2 g CH3OH、0.2 g NaOH,溶解后向其中加入20 g(0.021~0.023 mol)菜籽油及60 mL正己烷。

②加熱至60~65 ℃,攪拌2.5~3 h,靜置。上層為生物柴油、正己烷及甲醇,下層主要為甘油。
③分液、水洗。
④蒸餾,保持120℃時至無液體流出,剩余物為生物柴油。
(1)步驟①中控制n(CH3OH)/n(油脂)>3的目的是________;正己烷的作用是________。
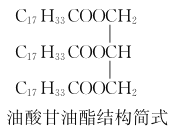
(2)步驟②適宜的加熱方式是________;菜籽油的成分之一油酸甘油酯(結構簡式如右圖)與甲醇反應的化學方程式為________________________________________________。
(3)步驟③用分液漏斗分離時,獲取上層液體的方法是________;用水洗滌上層液體時,說明已洗滌干凈的依據是__________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知HF 和HCN 都是一元弱酸,但Ka(HF)>Ka(HCN)。現有100mL0.1mol/L 的NaF 溶液(代號“甲”)和100mL 0.1mol/L 的NaCN 溶液(代號“乙”),下列有關甲、乙兩種溶液的說法中不正確的是( )
A. 溶液pH:甲<乙 B. 溶液中弱酸分子濃度:c(HF)>c(HCN)
C. 甲溶液中:c(HF)=c(OH-)-c(H+) D. 乙溶液中: c(Na+)=c(CN-)+c(HCN)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定條件下,利用如圖所示裝置可實現有機物的儲氫,下列有關說法正確的是( )
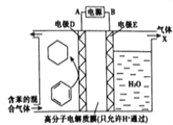
A. 氣體X是氫氣,電極E是陰極
B. H+由左室進入右室,發生還原反應
C. 該儲氫過程就是C6H6與氫氣反應過程
D. 電極D的電極反應式為C6H6+6H++6e-=C6H12
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】第VA族元素單質及其化合物在生產、生活中有重要的用途。
(1)下列說法正確的是__________(填序號)。
a.含氧酸的酸性:HNO3>H3PO4>H3AsO4 b.原子半徑:S >P>As
c.氫化物的穩定性NH3>PH3> AsH3d.AsH3電子式是![]()
(2)雌黃(As2S3 )和雄黃(As4S4)都是自然界中常見的砷化物,早期都曾用作繪畫顏料,因都有抗病毒療效也用來入藥。砷元素有+2、+3兩種常見價態。一定條件下,雌黃和雄黃的轉化關系如圖所示。
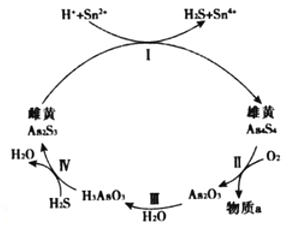
①Ⅱ中若1molAs4S4反應轉移28mole-,a物質是__________。
②Ⅰ中反應的離子方程式是____________________________________。
(3)亞砷酸(H3AsO3)可以用于治療白血病,其在溶液中存在多種微粒形態,各種微粒物質的量分數與溶液的pH關系如圖所示。

①人體血液的pH在7.35~7.45 之間,用藥后人體中含砷元素的主要微粒是___________。
②H3AsO3的一級電離常數是6×10-10mol·L-1,n(H3AsO3)∶n(H2AsO3-)=1∶1時,溶液的pH=___________(列出計算式即可)。
(4)由輝鉍礦(主要成分為Bi2S3,含雜質PbO2等)制備Bi2O3的工藝如圖所示:

①“浸出”時Bi2S3與FeCl3 溶液反應的離子方程式為________________________________。
②“置換”時生成單質鉍的離子方程式為____________________________________。
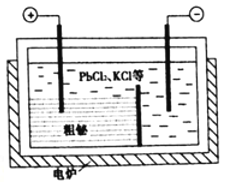
③“粗秘”中含有的雜質主要是Pb,通過熔融鹽電解精煉可達到除雜的目的,其裝置示意圖如所示。電解后陽極底部留下的為精鉍。寫出陽極電極反應的方程式__________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關溶液中微粒的物質的量濃度關系正確的是( )
A. 某弱酸的酸式鹽NaHA溶液中一定有:c(OH﹣)+2c(A2﹣)=c(H+)+c(H2A)
B. 0.2 molL﹣1 CH3COONa溶液與0.1 molL﹣1鹽酸等體積混合后的酸性溶液中:c(CH3COO﹣)>c(CH3COOH)>c(Cl﹣)>c(H+)
C. 室溫下,向100ml0.5mol/L的Na2CO3溶液中加入0.05molCaO,  溶液中增大
溶液中增大
D. 0.1 molL﹣1(NH4)2Fe(SO4)2溶液中:c(NH4+)+c(NH3H2O)+c(Fe2+)=0.3 molL﹣1
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com