
| A. | 若Ⅰ達平衡時,A、B、C各增加1mol,則A的轉化率將一定增大 | |
| B. | 若向Ⅰ平衡體系中再加入1molA和3molB,C的體積分數若大于x,可斷定n>3 | |
| C. | 若Ⅱ體系起始物質的量當滿足9a+c=3b,則可判斷n=3 | |
| D. | 若n=2,則Ⅱ體系起始物質的量應滿足1<b<3 |
分析 在恒溫恒容的密閉容器中,將1molA和3molB在一定條件下反應,達平衡時C的體積分數為x,若起始時A、B、C投入的物質的量分別為a、b、c,平衡時C的體積分數也為x,二者應為等效平衡,應存在a+$\frac{1}{n}$c=1,b+$\frac{2}{n}$c=3,以此解答該題.
解答 解:在恒溫恒容的密閉容器中,將1molA和3molB在一定條件下反應,達平衡時C的體積分數為x,若起始時A、B、C投入的物質的量分別為a、b、c,平衡時C的體積分數也為x,二者應為等效平衡,應存在a+$\frac{1}{n}$c=1,b+$\frac{2}{n}$c=3,
A.由于n值不確定,則若Ⅰ達平衡時,A、B、C各增加1mol,B的轉化率不能確定,故A錯誤;
B.因容器體積不變,若x=3時,C的體積分數應為x,現大于x,x應小于3,促進平衡正向移動,故B錯誤;
C.由恒溫恒容時,當a、b、c為起始物質的量,平衡時C的體積分數仍為x,a+$\frac{1}{n}$c=1,b+$\frac{2}{n}$c=3,若n=3,二者聯式可得9a+c=3b,故C正確;
D.由恒溫恒容時,當a、b、c為起始物質的量,平衡時C的體積分數仍為x,a+$\frac{1}{n}$c=1,b+$\frac{2}{n}$c=3,若n=2,二者聯式可得b=2a+1,由于0<a<1,則1<b<3,故D正確;
故選CD.
點評 本題考查化學平衡的計算,題目難度較大,注意從等效平衡的角度解答該題,易錯點為A,注意n不確定,A、B、C各增加1mol,B的轉化率可能增加,也可能不變.


科目:高中化學 來源: 題型:解答題
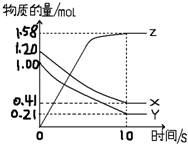 一定溫度下,在2L的密閉容器中,X、Y、Z三種氣體的物質的量隨時間變化的曲線如圖所示:
一定溫度下,在2L的密閉容器中,X、Y、Z三種氣體的物質的量隨時間變化的曲線如圖所示:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 氫氧化鈉與鹽酸;氫氧化銅與鹽酸 | B. | BaCl2與Na2SO4;Ba(OH)2與H2SO4 | ||
| C. | Na2CO3與硝酸;CaCO3與硝酸 | D. | 石灰石與硝酸反應;石灰石與鹽酸 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | NaA的溶液呈堿性 | B. | pH=2的HA溶液稀釋100倍后pH=3.5 | ||
| C. | 0.01 mol•Lˉ1HA溶液的pH=4 | D. | HA溶液跟鋅反應,放出H2很慢 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
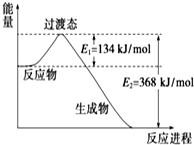 (1)如圖是NO2和CO反應生成CO2和NO過程中能量變化示意圖,請寫出NO2和CO反應的熱化學方程式:NO2(g)+CO(g)=CO2(g)+NO(g)△H=-234KJ/mol.
(1)如圖是NO2和CO反應生成CO2和NO過程中能量變化示意圖,請寫出NO2和CO反應的熱化學方程式:NO2(g)+CO(g)=CO2(g)+NO(g)△H=-234KJ/mol.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 2A+3B=2C | B. | A+3B2=C | C. | 3A+B=2C | D. | A+B=C |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | K+、Na+、SO42-、NO3- | B. | Na+、K+、ClO-、CO32- | ||
| C. | Fe2+、Mg2+、Cl-、SO42- | D. | NH4+、Cl-、K+、SO32- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | X2被還原,X2是還原劑 | B. | Y2被氧化,Y2是氧化劑 | ||
| C. | X2被氧化,X2是還原劑 | D. | Y2被氧化,Y2是還原劑 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com