
| A. | 0.5mol/L | B. | 5mol/L | C. | 10mol/L | D. | 20mol/L |
 階梯計算系列答案
階梯計算系列答案科目:高中化學 來源: 題型:選擇題
| 反應時間/min | n(CO)/mol | n(H2O)/mol |
| 0 | 1.20 | 0.60 |
| t1 | 0.80 | |
| t2 | 0.20 |
| A. | 反應在t1 min內的平均速率為v(H2)=$\frac{0.40}{{t}_{1}}$mol•L-1•min-1 | |
| B. | 保持其他條件不變,起始時向容器中充入0.60mol CO和1.20mol H2O,到達平衡時n(CO2)=0.40mol | |
| C. | 保持其他條件不變,向平衡體系中再通入0.20mol H2O(g),△H增大 | |
| D. | 溫度升高至800℃,上述反應平衡常數為0.64,則正反應為吸熱反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | CH3COOH | B. | H2CO3 | C. | HCN | D. | HClO |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①③④⑤ | B. | ②③④⑥ | C. | ③④⑤⑥ | D. | ②③④⑤ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
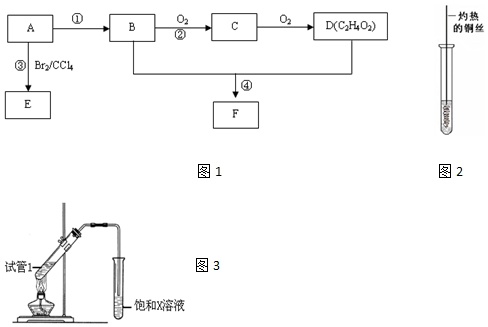
 ,D中官能團為羧基(-COOH).
,D中官能團為羧基(-COOH). CH3COOCH2CH3+H2O.
CH3COOCH2CH3+H2O.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com