
| A. | 用丙烷和水蒸氣高溫下反應制取氫氣,每產生0.3molCO,同時產生0.7NA個H2分子 | |
| B. | 常溫常壓下,16 g O3所含的電子數為8NA | |
| C. | 標準狀況下 11.2 L NO與11.2 L O2混合,充分反應后所含分子數小于0.75NA | |
| D. | 1 mol/L的Ca(ClO)2溶液中含ClO-數目一定小于2NA |
分析 A.依據方程式:C3H8+3H2O=3CO+7H2解答;
B.質量轉化為物質的量,結合1個臭氧分子含有24個電子解答;
C.11.2LNO與11.2LO2混合后發生的反應為2NO+O2═2NO2,2NO2 N2O4,則反應后的氣體的物質的量小于0,75mol;
N2O4,則反應后的氣體的物質的量小于0,75mol;
D.溶液體積未知,無法計算.
解答 解:A.用丙烷和水蒸氣高溫下反應制取氫氣,方程式為:C3H8+3H2O=3CO+7H2,依據反應物的物質的量之比等于計量系數之比,每產生0.3molCO,同時產生0.7mol氫氣分子即0.7NA個H2分子,故A正確;
B.常溫常壓下,16 g O3的物質的量$\frac{16g}{48g/mol}$=$\frac{1}{3}$mol,含有電子數為$\frac{1}{3}$×24×NA=8NA,故B正確;
C.11.2LNO與11.2LO2混合后發生的反應為2NO+O2═2NO2,2NO2 N2O4,則反應后的氣體的物質的量小于0,75mol,混合后所含分子數目小于0.75NA,故C正確;
N2O4,則反應后的氣體的物質的量小于0,75mol,混合后所含分子數目小于0.75NA,故C正確;
D.溶液體積未知,無法計算次氯酸根的數目,故D錯誤;
故選:D.
點評 本題考查了阿伏伽德羅常數的綜合應用,題目難度中等,注意掌握標況下氣體摩爾體積的使用條件,明確物質的量與阿伏伽德羅常數、摩爾質量等物理量之間的轉化關系.


科目:高中化學 來源: 題型:解答題
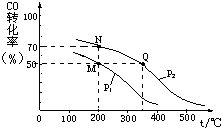 開發新能源和三廢處理都是可持續發展的重要方面.
開發新能源和三廢處理都是可持續發展的重要方面.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | B和C可形成一種含不同類型的化學鍵的堿性氧化物 | |
| B. | D2-離子在水溶液中與Al3+、H+均不能大量共存 | |
| C. | A2B的穩定性強于A2D的穩定性 | |
| D. | A2D和DB2可發生氧化還原反應,其中氧化產物與還原產物的物質的量之比為2:1 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | X=0.6mol | |
| B. | 離子的物質的量關系滿足n(Cl-)=5n(ClO-)+n(ClO3-) | |
| C. | 若反應中轉移的電子為n mol,則有0.3<n<0.5 | |
| D. | ClO3-的物質的量范圍是:0.1mol<n(ClO3-)<0.3mol |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. |  用圖裝置萃取溴水中的溴,并把溴的苯溶液從下口放出 | |
| B. |  用圖裝置可以驗證溴乙烷發生了消去反應 | |
| C. |  用圖裝置配制銀氨溶液 | |
| D. |  用圖裝置可說明濃H2SO4具有脫水性、強氧化性,SO2具有漂白性、還原性 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
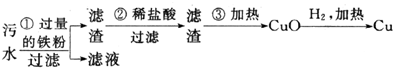
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在FeCl3溶液中滴入幾滴KSCN溶液,溶液變成血紅色 | |
| B. | 淡黃色溴化銀見光分解后變成白色 | |
| C. | 向血紅色的Fe(SCN)3溶液中加入少量KI固體,溶液顏色變淺 | |
| D. | 用50mL針筒抽取30mL紅棕色的NO2氣體并封住注射孔,當用力推壓活塞,壓縮針筒中的氣體(此過程不考慮溫度變化),氣體顏色逐漸變深 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 氧化鐵能與酸反應,可用于制成紅色涂料或顏料 | |
| B. | 煙花的絢麗繽紛是含鉀、鈉、鈣、銅等金屬元素的化合物的化學性質的展現 | |
| C. | 醫用酒精是用淀粉類植物經糖化再發酵經蒸餾制成,濃度通常是75% | |
| D. | 維生素C是水溶性維生素,能增強人體抵抗力,有抗氧化作用 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com