
| A. | NF3分子呈三角錐形 | |
| B. | NF3分子是極性分子 | |
| C. | NF3與NH3晶體類型相同 | |
| D. | 上述反應的反應物和生成物均屬于共價分子 |
分析 A.根據(jù)NH3分子構(gòu)型判斷NF3分子構(gòu)型;
B.分子結(jié)構(gòu)不對稱,正負電荷中心不重疊,則為極性分子,反之為非極性分子;
C.NF3與NH3都為分子晶體;
D.NH4F含銨根離子、氟離子,是離子化合物.
解答 解:A.氨氣分子中價層電子對個數(shù)=σ鍵個數(shù)+孤電子對個數(shù)=3+$\frac{1}{2}$(5-3×1)=4,所以氮原子雜化方式是sp3,因為含有一個孤電子對,所以是三角錐型結(jié)構(gòu),NF3分子構(gòu)型與NH3相似,所以NF3分子構(gòu)型也是三角錐型的,故A正確;
B.NF3分子構(gòu)型與NH3相似,NH3分子構(gòu)型是三角錐型的,所以NF3分子構(gòu)型也是三角錐型的,三角錐形分子的結(jié)構(gòu)不對稱,正負電荷中心不重疊,為極性分子,故B正確;
C.NF3存在N-F鍵,NH3存在N-H鍵,都為分子晶體,NF3與NH3晶體類型相同,故C正確;
D.氨氣、氟氣以及NF3為分子晶體,NH4F中存在的化學鍵是離子鍵、共價鍵,NH4F是離子化合物,故D錯誤;
故選D.
點評 本題考查物質(zhì)的結(jié)構(gòu)、化學鍵、物質(zhì)的分類等知識,類推方法的應用是解答的關鍵,題目難度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:解答題
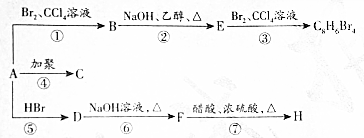
 ,D
,D ,E
,E .
. +2NaOH$→_{△}^{醇}$
+2NaOH$→_{△}^{醇}$ +2NaBr+2H2O(消去反應).
+2NaBr+2H2O(消去反應). +NaOH$→_{△}^{水}$
+NaOH$→_{△}^{水}$ +NaBr(取代反應).
+NaBr(取代反應).查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 生成的正鹽化學式為BmAn | |
| B. | 該鹽中存在著一定水解的離子,該離子水解方程式為:Bm++mH2O?B(OH)m+mH+ | |
| C. | 生成的鹽為強酸弱堿鹽 | |
| D. | HnA為弱酸,其第一步電離方程式為:HmA?Hm-1A-+H+ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | CH3Br | B. | CH3CH2CH2CH2Br | ||
| C. | CH3CHBrCH2Br | D. | BrCH2CH2CH2CH2Br |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 廢舊塑料露天焚燒 | B. | 用廚房垃圾生產(chǎn)沼氣 | ||
| C. | 廢舊電池就地填埋 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 原電池中失去電子的電極為陽極 | |
| B. | 原電池的兩極一定是由活動性不同的兩種金屬組成 | |
| C. | 電解時電解池的陽極一定是陰離子放電 | |
| D. | 原電池的負極、電解池的陽極都發(fā)生氧化反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
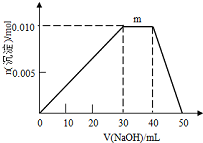 化學與人類社會可持續(xù)發(fā)展密切相關,能源、環(huán)境、材料以及日常生活等離不開化學.
化學與人類社會可持續(xù)發(fā)展密切相關,能源、環(huán)境、材料以及日常生活等離不開化學.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 鹵素單質(zhì)與水反應的通式為X2+H2O?HX+HXO | |
| B. | HX都極易溶于水,它們的熱穩(wěn)定性隨核電荷數(shù)增大而增強 | |
| C. | 鹵素單質(zhì)的顏色隨相對分子質(zhì)量增大的順序而加深 | |
| D. | X-離子的還原性依次為:F-<Cl-<Br-<I-,因此相對分子質(zhì)量小的鹵素單質(zhì)可將相對分子質(zhì)量大的鹵素從它的鹽溶液里置換出來 |
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權(quán)舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com