
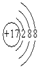

 ,化合物中含有離子鍵鍵(填離子或共價)
,化合物中含有離子鍵鍵(填離子或共價)分析 短周期元素A、B、C、D中,0.5mol A元素的離子得到NA個電子被還原為中性原子,則A離子帶兩個單位正電荷,0.4g A的氧化物恰好與100ml 0.2mol/L的鹽酸完全反應,HCl的物質的量=0.1L×0.2mol/L=0.02mol,由AO+2HCl═ACl2+H2O,可知0.4gAO的物質的量為0.01mol,則M(AO)=$\frac{0.4g}{0.01mol}$=40g/mol,故A的摩爾質量為40g/mol-16g/mol=24g/mol,A原子核內質子數目與中子數目相等,則質子數為12,即A為Mg元素;B元素原子核外電子數比A元素原子核外電子數多1,則B為Al;C-比A元素的離子多1個電子層,則C的質子數為18-1=17,即C為Cl元素;D元素原子最外層電子數是次外層電子數的2倍,原子只能有2個電子層,最外層電子數為4,即D為C元素,以此解答.
解答 解:短周期元素A、B、C、D中,0.5mol A元素的離子得到NA個電子被還原為中性原子,則A離子帶兩個單位正電荷,0.4g A的氧化物恰好與100ml 0.2mol/L的鹽酸完全反應,HCl的物質的量=0.1L×0.2mol/L=0.02mol,由AO+2HCl═ACl2+H2O,可知0.4gAO的物質的量為0.01mol,則M(AO)=$\frac{0.4g}{0.01mol}$=40g/mol,故A的摩爾質量為40g/mol-16g/mol=24g/mol,A原子核內質子數目與中子數目相等,則質子數為12,即A為Mg元素;B元素原子核外電子數比A元素原子核外電子數多1,則B為Al;C-比A元素的離子多1個電子層,則C的質子數為18-1=17,即C為Cl元素;D元素原子最外層電子數是次外層電子數的2倍,原子只能有2個電子層,最外層電子數為4,即D為C元素,
(1)綜上所述,A為Mg,B為Al,名稱分別為鎂和鋁,故答案為:鎂;鋁;
(2)Cl的質子數為17,離子結構示意圖為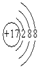 ,故答案為:
,故答案為: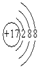 ;
;
(3)D為碳元素,最高價氧化物為CO2,分子中C原子與O原子之間形成2對共用電子對,其電子式為: ,故答案為:
,故答案為: ;
;
(4)Cl、Mg兩元素形成的化合物為MgCl2,MgCl2屬于離子化合物,Mg最外層兩個電子被兩個Cl原子得到,用電子式表示形成過程為: ,故答案為:
,故答案為: ;
;
(5)Al與氫氧化鈉反應生成偏鋁酸鈉和氫氣,離子反應方程式為:2Al+2OH-+2H2O=2AlO2-+3H2↑,故答案為:2Al+2OH-+2H2O=2AlO2-+3H2↑.
點評 本題考查位置結構性質關系及其應用,側重對化學用語的考查,推斷元素是解答關鍵,題目難度中等.


科目:高中化學 來源: 題型:多選題
| A. | 電解水:2H20=2H2↑+O2↑ | B. | 4Fe(OH)2+O2+2H2O=4Fe(OH)3 | ||
| C. | 2F2+H2O=4HF+O2 | D. | 3NO2+H2O=2HNO3+NO |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
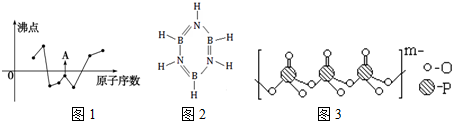
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 電離常數隨著弱電解質濃度的增大而增大 | |
| B. | CH3COOH的電離常數表達式為Ka=$\frac{c(C{H}_{3}COOH)}{c({H}^{+})•c(C{H}_{3}CO{O}^{-})}$ | |
| C. | 電離常數只受溫度影響,與濃度無關 | |
| D. | CH3COOH溶液中加入少量CH3COONa固體,電離常數減小 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 非金屬性:F>Cl>Br>I | B. | 單質氧化性:F2>Cl2>Br2>I2 | ||
| C. | 氫化物穩定性:HF>HCl>HBr>HI | D. | 沸點:F2>Cl2>Br2>I2 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題


 (苯胺,弱堿性,易氧化)
(苯胺,弱堿性,易氧化)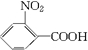 .
. .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 聚氯乙烯一次性超薄袋可用于包裝食品 | |
| B. | 利用電滲析法和離子交換法能獲得純凈水 | |
| C. | 體積分數為95%的酒精用作醫用酒精 | |
| D. | 石油裂化的目的是得到乙烯、丙烯等化工原料 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 大于零即可 | B. | 大于0.6mol | C. | 大于或等于1mol | D. | 任意值 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com