
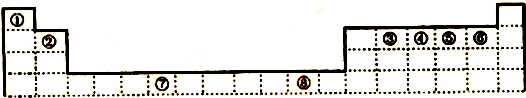
| 1 |
| 1 |
| 6 |
| 12 |
| 16 |
| 16 |
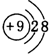 ,
, ;
;| 1 |
| 1 |
| 6 |
| 12 |
| 16 |
| 16 |
| 6-3×2 |
| 2 |


科目:高中化學 來源: 題型:
| 選項 | 實驗目的 | 玻璃儀器 |
| A | 配制一定質量分數的NaCl溶液 | 膠頭滴管、量筒、燒杯、玻璃棒 |
| B | 測定NaOH溶液濃度 | 滴定管、錐形瓶、燒杯 |
| C | 鑒別葡萄糖和蔗糖 | 試管、燒杯、酒精燈 |
| D | 實驗室用濃氨水和生石灰制備氨氣 | 普通漏斗、燒杯、玻璃棒 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、1 mol/(L?min) |
| B、2mol/(L?min) |
| C、4 mol/(L?min) |
| D、8mol/(L?min) |
查看答案和解析>>
科目:高中化學 來源: 題型:
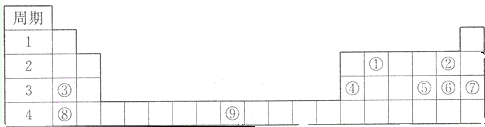
查看答案和解析>>
科目:高中化學 來源: 題型:

查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
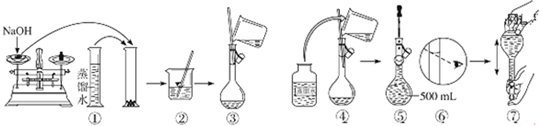
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com