
| A. | 氧化性強弱順序為XO42->Z2>R2>M3+ | |
| B. | Z2在③中發生氧化反應 | |
| C. | R元素在反應②中被氧化,在③中被還原 | |
| D. | 常溫下反應不可進行2M2++Z2═2M3++2Z- |
分析 ①H++Z-+XO42-→X2++Z2+H2O,反應中XO4-是氧化劑,Z2是氧化產物,氧化性:XO4->Z2;
②2M2++R2═2M3++2R-,反應中R2是氧化劑,M3+是氧化產物,氧化性:R2>M3+;
③2R-+Z2═R2+2Z-,反應中Z2是氧化劑,R2是氧化產物,氧化性:Z2>R2;
所以氧化性強弱關系為:XO4->Z2>R2>M3+,以此解答該題.
解答 解:①H++Z-+XO42-→X2++Z2+H2O,反應中XO4-是氧化劑,Z2是氧化產物,氧化性:XO4->Z2;
②2M2++R2═2M3++2R-,反應中R2是氧化劑,M3+是氧化產物,氧化性:R2>M3+;
③2R-+Z2═R2+2Z-,反應中Z2是氧化劑,R2是氧化產物,氧化性:Z2>R2;
所以氧化性強弱關系為:XO4->Z2>R2>M3+,
A.所以氧化性強弱關系為:XO4->Z2>R2>M3+,故A正確;
B.③2R-+Z2═R2+2Z-,反應中Z2是氧化劑,發生還原反應,故B錯誤;
C.R元素在反應②中做氧化劑,被還原,在③中做還原劑,被氧化,故C錯誤;
D.反應2M2++Z2═2M3++2Z-中,Z2是氧化劑,M3+是氧化產物,氧化性Z2>M3+,符合題意,故D錯誤;
故選:A.
點評 本題考查了氧化性、還原性強弱比較,明確氧化還原反應強弱規律,準確判斷氧化劑、氧化產物、還原劑、還原產物是解題關鍵,題目難度不大.


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:填空題
| 物質 | CH3OH | CH3OCH3 | H2O |
| c/mol•L-1 | 0.44 | 0.60 | 0.60 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
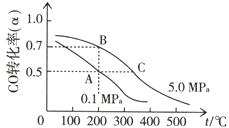 “潔凈煤技術”研究在世界上相當普遍,科研人員通過向地下煤層氣化爐中交替鼓入空氣和水蒸氣的方法,連續產出了熱值高達122500~16000kJ•m-3的煤炭氣,其主要成分是CO和H2.CO和H2可作為能源和化工原料,應用十分廣泛.
“潔凈煤技術”研究在世界上相當普遍,科研人員通過向地下煤層氣化爐中交替鼓入空氣和水蒸氣的方法,連續產出了熱值高達122500~16000kJ•m-3的煤炭氣,其主要成分是CO和H2.CO和H2可作為能源和化工原料,應用十分廣泛.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 提高風能、太陽能等可再生清潔能源的使用比例 | |
| B. | 推廣CO2再利用技術,將其合成有價值的化學品 | |
| C. | 利用工業廢水灌溉農作物,提高水資源的利用率 | |
| D. | 研發煤炭的潔凈、高效利用技術,保護生態環境 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 石蕊,由藍變紅 | B. | 酚酞,紅色褪去 | C. | 甲基橙,由黃變橙 | D. | 甲基橙,由橙變黃 |
查看答案和解析>>
科目:高中化學 來源: 題型:計算題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 通入22.4LSO2參加反應時,有2 NA個電子發生轉移 | |
| B. | 上述實驗條件下,物質的氧化性:Cu2+>I2>SO2 | |
| C. | 滴加KI溶液時,KI被氧化,CuI是氧化產物 | |
| D. | 通入SO2后溶液逐漸變成無色,體現了SO2的漂白性 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | CO2通入CaCl2溶液中 | B. | NO2通入FeSO4溶液中 | ||
| C. | NH3通入A1C13溶液中 | D. | SO2通入Ba(NO3)2溶液中 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| t/℃ | 0 | 10 | 20 | 25 | 40 | 50 | 100 |
| KW/10-14 | 0.114 | 0.292 | 0.681 | 1.00 | 2.92 | 5.47 | 55.0 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com