
| A. | 一定是ⅠA族元素 | |
| B. | 一定是金屬元素 | |
| C. | 可能不是金屬元素也可能是非金屬元素 | |
| D. | 不是ⅡA族元素就是副族元素 |
 口算能手系列答案
口算能手系列答案科目:高中化學 來源: 題型:選擇題
| A. | 若a=b且pH(NaX)>pH(NaY),則酸性HX<HY | |
| B. | 若a=b且c(X -)=c(Y -)+c(HY),則酸性HX>HY | |
| C. | 若a>b且c(X -)=c(Y -),則酸性HX<HY | |
| D. | 若a=0.1mol/L且兩溶液等體積混合,則c(X -)+c(HX)=0.1mol/L |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
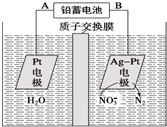
| A. | 鉛蓄電池的A極為正極,電極材料為PbO2 | |
| B. | 該電解池的總反應方程式為:2H2O+4NO3- $\frac{\underline{\;電解\;}}{\;}$2N2↑+5O2↑+4OH- | |
| C. | 該電解池的陰極反應式為:2NO3-+12H++10e-═N2↑+6H2O | |
| D. | 若電解過程中轉移2mol電子,則交換膜右側電解液的質量減少5.6g |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 它們的原子序數B>A>C | B. | 它們的離子半徑A2->C->B2+ | ||
| C. | 它們的原子半徑C>B>A | D. | 它們的最外層電子數C>A>B |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
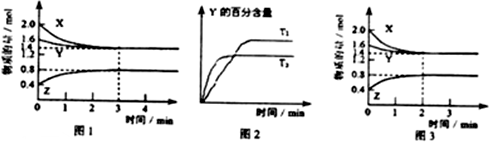
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
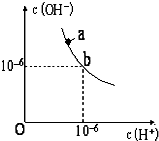 回答下列問題.
回答下列問題.查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 23g Na在空氣中完全燃燒,轉移的電子數為1 mol | |
| B. | 78gNa2O2含有的離子數為3NA | |
| C. | 0.1 mol Fe與足量水蒸氣反應生成H2的分子數為0.1NA | |
| D. | 5.4 g鋁與足量NaOH溶液反應,產生6.72L的氫氣 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | pH=5.6的CH3COOH與CH3COONa混合溶液:c(Na+)>c(CH3COO-)>c(CH3COOH)>c(H+)>c(OH-) | |
| B. | 常溫下,向0.01mol/L NH4HSO4溶液中滴加NaOH溶液至中性:c(Na+)>c(SO42-)>c(NH4+)>c(H+)=c(OH-) | |
| C. | NaHCO3溶液:c(OH-)+c(CO32-)=c(H+)+c(H2CO3) | |
| D. | 濃度均為0.1mol/L的①NH4Cl ②NH3•H2O ③NH4HSO4 ④NH4HCO3四種溶液,c(NH4+)由大到小的順序為:③>①>④>② |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com