
| 選項 | 化學反應及離子方程式 | 評價 |
| A | AlCl3溶液中加入過量氨水: Al3++3NH3•H2O═Al(OH)3↓+3NH4+ | 錯誤,鋁元素的產物應該是AlO2- |
| B | 過量氯氣通入溴化亞鐵溶液中: 3Cl2+2Fe2++4Br-═6Cl-+2Fe3++2Br2 | 正確 |
| C | 用氨水吸收過量二氧化硫: 2NH3•H2O+SO2═2NH4++SO32-十H2O | 正確 |
| D | 氯化銨溶于水: NH4++2H2O═H3O++NH3•H2O | 錯誤,氯化銨溶解于水是物理變化,不能寫離子方程式 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.氯化鋁溶液中加入過量的氨水,氫氧化鋁不溶于氨水,該離子方程式正確,評價錯誤;
B.氯氣過量,亞鐵離子和溴離子都被氧化;
C.二氧化硫過量,反應生成與硫酸氫銨;
D.銨根離子的水解的離子方程式應該用可逆號.
解答 解:A.氫氧化鋁不溶于氨水,二者反應的離子方程式為:Al3++3NH3•H2O═Al(OH)3↓+3NH4+,題中離子方程式正確,評價不合理,故A錯誤;
B.過量氯氣通入溴化亞鐵溶液中,亞鐵離子和溴離子都完全被氧化,反應的離子方程式為:3Cl2+2Fe2++4Br-═6Cl-+2Fe3++2Br2,題中評價合理,故B正確;
C.用氨水吸收過量二氧化硫,反應生成的是與硫酸氫銨,正確的離子方程式為:NH3•H2O+SO2═2NH4++HSO3-,題中離子方程式錯誤,評價錯誤,故C錯誤;
D.氯化銨溶于水,銨根離子發生水解,水解為可逆反應,正確的離子方程式為:NH4++2H2O?H3O++NH3•H2O,題中評價不合理,故D錯誤;
故選B.
點評 本題考查了常見化學用語的書寫及評價,題目難度中等,注意掌握離子方程式書寫原則、鹽的水解原理及其應用方法,本題中關鍵抓住題干要求“對化學用語的評價合理的是”,即只判斷評價是否合理,不是判斷離子方程式書寫是否正確,為易錯點.


科目:高中化學 來源:2016-2017學年江西省高二上月考一化學試卷(解析版) 題型:選擇題
一定溫度下,有可逆反應:2A(g)+2B(g) C(g)+3D(g);ΔH<0。現將2 mol A和2 mol B充入體積為V的甲容器,將2 mol C和6 mol D充入乙容器并使乙容器在反應開始前的體積為2V(如圖1)。
C(g)+3D(g);ΔH<0。現將2 mol A和2 mol B充入體積為V的甲容器,將2 mol C和6 mol D充入乙容器并使乙容器在反應開始前的體積為2V(如圖1)。
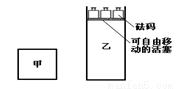
關于兩容器中反應的說法正確的是
A.兩容器達平衡后升高相同的溫度時,甲容器的反應速率大于乙容器的速率
B.兩容器中的反應均達平衡時,平衡混合物中各組份的體積百分組成相同,混合氣體的密度不同
C.甲容器中的反應先達到化學平衡狀態
D.在甲容器中再充入2mol A和2 mol B,平衡后甲中物質C的物質的量是乙中物質C的物質的量的2倍
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
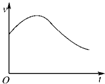 氯酸鉀和亞硫酸氫鈉發生氧化還原反應生成Cl(-1價)和S(+6價)的速率如圖所示,已知這個反應速率隨著溶液中c(H+)增大而加快.
氯酸鉀和亞硫酸氫鈉發生氧化還原反應生成Cl(-1價)和S(+6價)的速率如圖所示,已知這個反應速率隨著溶液中c(H+)增大而加快.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 ;
;查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | FeCl3溶液和KSCN溶液混合 | B. | 鋅放入稀硫酸中 | ||
| C. | 銅片放入氯化鐵溶液中 | D. | 硫酸銅溶液與氫氧化鈉溶液混合 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com