
(4分) 氮元素的氫化物和氧化物在工業生產和國防建設中都有廣泛應用,回答下列問題:
(1)NH3與NaClO反應可得到肼(N2H4),該反應的化學方程式為 ;
(2)肼可作為火箭發動機的燃料,與氧化劑N2O4反應生成N2和水蒸氣。
已知:①N2(g)+2O2(g)= N2O4 (1) △H1= -195kJ·mol-1
②N2H4 (1) + O2(g)= N2(g) + 2 H2O △H2= -534.2kJ·mol-1
寫出肼和N2O4反應的熱化學方程式 ;
科目:高中化學 來源:2013屆江西省上饒市橫峰中學高三第一次月考化學試卷(帶解析) 題型:填空題
(本題共12分)
Ⅰ、氮元素的氫化物和氧化物在工業生產和國防建設中都有廣泛應用。回答下列問題:
(1)氮元素原子的L層電子數為 ;
(2) NH3與NaClO反應可得到肼(N2H4),該反應的化學方程式為 ;
(3)肼可作為火箭發動機的燃料,與氧化劑N2O4反應生成N2和水蒸氣。
已知:①N2(g)+2O2(g) = N2O4(l) ΔH1=-19.5kJ?mol-1
②N2H4(l) + O2 (g)=N2(g)+2H2O(g) ΔH2 ="-534.2" kJ·mol-1
寫出肼和N2O4反應的熱化學方程式 ;
(4)肼一空氣燃料電池是一種堿性電池,該電池放電時,負極的反應式為 。
Ⅱ、一定質量的液態化合物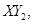 在標準狀況下的一定質量的
在標準狀況下的一定質量的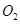 中恰好完全燃燒,反應方程式為:
中恰好完全燃燒,反應方程式為: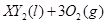 ===
===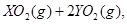 冷卻后,在標準狀況下測得生成物的體積是672 mL,密度是2.56
冷卻后,在標準狀況下測得生成物的體積是672 mL,密度是2.56 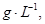 則:
則:
(1)反應前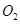 的體積是 。 (2)化合物
的體積是 。 (2)化合物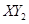 的摩爾質量是 。
的摩爾質量是 。
(3)若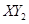 分子中X、Y兩元素的質量比是3∶16,則X、Y兩元素分別為 和 (寫元素符號)。
分子中X、Y兩元素的質量比是3∶16,則X、Y兩元素分別為 和 (寫元素符號)。
查看答案和解析>>
科目:高中化學 來源:2014屆安徽省高二10月月考化學試卷(解析版) 題型:填空題
(4分) 氮元素的氫化物和氧化物在工業生產和國防建設中都有廣泛應用,回答下列問題:
(1)NH3與NaClO反應可得到肼(N2H4),該反應的化學方程式為 ;
(2)肼可作為火箭發動機的燃料,與氧化劑N2O4反應生成N2和水蒸氣。
已知:①N2(g)+2O2(g)= N2O4 (1) △H1= -195kJ·mol-1
②N2H4 (1) + O2(g)= N2(g) + 2 H2O △H2= -534.2kJ·mol-1
寫出肼和N2O4 反應的熱化學方程式 ;
查看答案和解析>>
科目:高中化學 來源:2012-2013學年江西省上饒市高三第一次月考化學試卷(解析版) 題型:填空題
(本題共12分)
Ⅰ、氮元素的氫化物和氧化物在工業生產和國防建設中都有廣泛應用。回答下列問題:
(1)氮元素原子的L層電子數為 ;
(2) NH3與NaClO反應可得到肼(N2H4),該反應的化學方程式為 ;
(3)肼可作為火箭發動機的燃料,與氧化劑N2O4反應生成N2和水蒸氣。
已知:①N2(g)+2O2(g) = N2O4(l) ΔH1=-19.5kJ∙mol-1
②N2H4(l) + O2 (g)=N2(g)+2H2O(g) ΔH2 =-534.2 kJ·mol-1
寫出肼和N2O4反應的熱化學方程式 ;
(4)肼一空氣燃料電池是一種堿性電池,該電池放電時,負極的反應式為 。
Ⅱ、一定質量的液態化合物 在標準狀況下的一定質量的
在標準狀況下的一定質量的 中恰好完全燃燒,反應方程式為:
中恰好完全燃燒,反應方程式為: 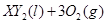 ===
===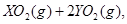 冷卻后,在標準狀況下測得生成物的體積是672 mL,密度是2.56
冷卻后,在標準狀況下測得生成物的體積是672 mL,密度是2.56  則:
則:
(1)反應前 的體積是
。
(2)化合物
的體積是
。
(2)化合物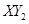 的摩爾質量是
。
的摩爾質量是
。
(3)若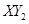 分子中X、Y兩元素的質量比是3∶16,則X、Y兩元素分別為
和
(寫元素符號)。
分子中X、Y兩元素的質量比是3∶16,則X、Y兩元素分別為
和
(寫元素符號)。
查看答案和解析>>
科目:高中化學 來源: 題型:
(13分)氮及其化合物在生產、生活和科技等方面有重要的應用,請回答下列問題:
(1)氮元素基態原子的價電子排布式為 ;
(2)在氮氣分子中,氮原子之間存在著 個![]() 鍵和 個
鍵和 個![]() 鍵;
鍵;
(3)磷、氮、氧是周期表中相鄰的三種元素,比較:(均填“大于”、“小于”或“等于”)
①氮原子的第一電離能 氧原子的第一電離能;
②N2分子中氮氮鍵的鍵長 白磷分子中磷磷鍵的鍵長;
(4)氮元素的氫化物(NH3)是一種易液化的氣體,請闡述其原因是 ;
(5)配合物[Cu(NH3)4]Cl2中含有4個配位鍵,若用2個N2H4代替其中的2個NH3,得到的配合物[Cu(NH3)2(N2H4)2]Cl2中含有配位鍵的個數為 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com