
| A. | 1molCl2溶于水反應,反應轉移電子數為nA | |
| B. | 56g晶體硅中含有硅分子數為2nA | |
| C. | 1 mol Cu和足量稀硝酸反應產生nA個NO分子 | |
| D. | 標準狀況下,1.12 L NO與1.12 L O2的混合物中含有的原子數為0.2nA |
分析 A、氯氣與水的反應為歧化反應;
B、晶體硅是原子晶體;
C、根據得失電子數守恒來分析;
D、標準狀況下,1.12 L NO與1.12 L O2的物質的量均為0.05mol,根據反應后原子個數守恒來分析.
解答 解:A、氯氣與水的反應為歧化反應,故1mol氯氣溶于水后轉移的電子數小于nA個,故A錯誤;
B、晶體硅是原子晶體,故在晶體硅中無硅分子,故B錯誤;
C、根據電子守恒計算,1molCu失2mole-,HNO3還原為NO,只生成$\frac{2}{3}$molNO,因此不應產生nA個NO分子,故C錯誤;
D、標準狀況下,1.12 L NO與1.12 L O2的物質的量均為0.05mol,而NO和氧氣均為雙原子分子,故0.05molNO和0.05mol氧氣中均含0.1mol原子,而兩者混合后發生反應生成二氧化氮,但由于反應過程中原子個數守恒,故混合后原子個數仍為0.2nA個,故D正確.
故選D.
點評 本題考查了阿伏伽德羅常數的有關計算,熟練掌握公式的使用和物質的結構是解題關鍵,難度不大.


科目:高中化學 來源: 題型:解答題
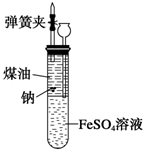 有人設計出一種在隔絕空氣條件下讓鈉與FeSO4溶液反應的方法以驗證反應實質.實驗時,往100mL大試管中先加40mL煤油,取3粒米粒大小的金屬鈉放入大試管后塞上橡皮塞,通過長頸漏斗加入用煮過的蒸餾水配制的FeSO4溶液使煤油的液面至膠塞,并夾緊彈簧夾(如圖).仔細觀察,回答下列問題:
有人設計出一種在隔絕空氣條件下讓鈉與FeSO4溶液反應的方法以驗證反應實質.實驗時,往100mL大試管中先加40mL煤油,取3粒米粒大小的金屬鈉放入大試管后塞上橡皮塞,通過長頸漏斗加入用煮過的蒸餾水配制的FeSO4溶液使煤油的液面至膠塞,并夾緊彈簧夾(如圖).仔細觀察,回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 標準狀況下,22.4L水含有NA個水分子 | |
| B. | 氧氣和臭氧的混合物32 g中含有NA個氧原子 | |
| C. | 0.1mol Na2O2與水反應時轉移0.1NA個電子 | |
| D. | 11.2 L氯氣中含有NA個氯原子 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
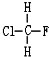 與
與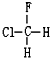 B.
B. 與
與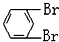 C.
C.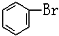 與
與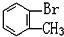 D.
D.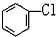 與
與 E.ClC(CH3)3與(CH3)2CHCH2Cl F.
E.ClC(CH3)3與(CH3)2CHCH2Cl F.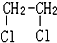 與CH3-CH2Cl
與CH3-CH2Cl 由一種單體脫水縮聚而成的,該單體的鍵線式為
由一種單體脫水縮聚而成的,該單體的鍵線式為
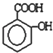 )滴入Na2CO3溶液中,生成的有機物的結構簡式是:
)滴入Na2CO3溶液中,生成的有機物的結構簡式是: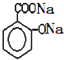
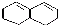 在較高溫度下和Br2按物質的量之比1:1發生1,4-加成反應的化學方程式
在較高溫度下和Br2按物質的量之比1:1發生1,4-加成反應的化學方程式 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 氨氣既能用濃硫酸干燥也能用無水CaCl2干燥 | |
| B. | NH3是電解質,所以氨水能導電 | |
| C. | 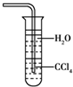 用水吸收NH3用如圖裝置可防止倒吸 | |
| D. | NH3可以使干燥的紅色石蕊試紙變藍 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 二氧化碳和氮氣 | B. | 二氧化碳和二氧化氮 | ||
| C. | 二氧化碳和氧氣 | D. | 氮氣和氧氣 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
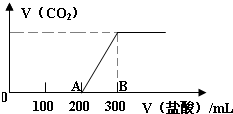 向100mL 3mol/L的NaOH溶液中緩慢通入一定量的CO2,充分反應,測得最后溶液的PH>7.
向100mL 3mol/L的NaOH溶液中緩慢通入一定量的CO2,充分反應,測得最后溶液的PH>7.查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com