
分析 Ⅰ.根據(jù)電池裝置,F(xiàn)e做負極放電,正極上高鐵酸鉀發(fā)生還原反應,均生成相同價態(tài)的化合物,高鐵酸鉀的氧化性很強,能夠生成三價鐵.
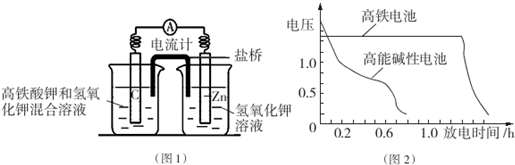
Ⅰ.(1)根據(jù)電池裝置,Zn做負極,C為正極,高鐵酸鉀的氧化性很強,正極上高鐵酸鉀發(fā)生還原反應生成Fe(OH)3;根據(jù)電子轉(zhuǎn)移計算Zn的質(zhì)量;
(2)鹽橋可起到平衡電荷,陰離子向負極移動,陽離子向正極移動;
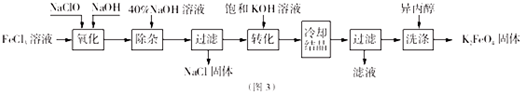
(3)由圖可知高鐵電池的優(yōu)點有:使用時間長、工作電壓穩(wěn)定;
Ⅱ.氯化鐵溶液中加入次氯酸鈉和氫氧化鈉,發(fā)生反應為:2FeCl3+10NaOH+3NaClO=2Na2FeO4+9NaCl+5H2O,將Na2FeO4粗產(chǎn)品在40%KOH溶液中溶解,過濾除去雜質(zhì)NaCl,加入飽和KOH溶液后,將Na2FeO4轉(zhuǎn)化為溶解度更小的K2FeO4,反應方程式為Na2FeO4+2KOH=K2FeO4+2NaOH,冷卻結(jié)晶、過濾,高鐵酸鉀易溶于水,難溶于異丙醇,用異丙醇代替水洗滌產(chǎn)品可以減少高鐵酸鉀的損耗,同時洗去高鐵酸鉀晶體表面的KOH和其他雜質(zhì),得到純產(chǎn)品高鐵酸鉀.
(4)其中Fe元素化合價由+3價升高為+6價,共升高3價,Cl元素化合價由+1價降低為-1,價,共降低2價,化合價升降最小公倍數(shù)為6,則FeCl3的系數(shù)為2、NaClO的系數(shù)為3,再根據(jù)原子守恒配平;所含元素化合價降低的反應物是氧化劑;
(5)加入飽和KOH溶液可以增大K+的濃度,減小高鐵酸鉀的溶解,促進高鐵酸鉀晶體析出;
(6)根據(jù)Ksp[Fe(OH)3]=c(Fe3+)×c3(OH-)=4.0×10-38計算開始沉淀時c(OH-),再根據(jù)水的離子積計算溶液中c(H+),根據(jù)稀釋定律計算需要鹽酸的體積;
解答 解:Ⅰ.(1)根據(jù)電池裝置,Zn做負極,C為正極,高鐵酸鉀的氧化性很強,正極上高鐵酸鉀發(fā)生還原反應生成Fe(OH)3,正極電極反應式為:FeO42-+4H2O+3e-═Fe(OH)3↓+5OH-,若維持電流強度為1A,電池工作十分鐘,通過電子為$\frac{1A×600s}{96500C/mol}$,則理論消耗Zn為$\frac{1A×600s}{96500C/mol}$×$\frac{1}{2}$×65g/mol=0.2g,
故答案為:FeO42-+4H2O+3e-═Fe(OH)3↓+5OH-;02;
(2)鹽橋中陰離子移向負極移動,鹽橋起的作用是使兩個半電池連成一個通路,使兩溶液保持電中性,起到平衡電荷,構(gòu)成閉合回路,放電時鹽橋中氯離子向右移動,用某種高分子材料制成陽離子交換膜代替鹽橋,則鉀離子向左移動,
故答案為:右;左;
(3)由圖可知高鐵電池的優(yōu)點有:使用時間長、工作電壓穩(wěn)定,
故答案為:使用時間長、工作電壓穩(wěn)定;
Ⅱ.氯化鐵溶液中加入次氯酸鈉和氫氧化鈉,發(fā)生反應為:2FeCl3+10NaOH+3NaClO=2Na2FeO4+9NaCl+5H2O,將Na2FeO4粗產(chǎn)品在40%KOH溶液中溶解,過濾除去雜質(zhì)NaCl,加入飽和KOH溶液后,將Na2FeO4轉(zhuǎn)化為溶解度更小的K2FeO4,反應方程式為Na2FeO4+2KOH=K2FeO4+2NaOH,冷卻結(jié)晶、過濾,高鐵酸鉀易溶于水,難溶于異丙醇,用異丙醇代替水洗滌產(chǎn)品可以減少高鐵酸鉀的損耗,同時洗去高鐵酸鉀晶體表面的KOH和其他雜質(zhì),得到純產(chǎn)品高鐵酸鉀.
(4)其中Fe元素化合價由+3價升高為+6價,共升高3價,Cl元素化合價由+1價降低為-1,價,共降低2價,化合價升降最小公倍數(shù)為6,則FeCl3的系數(shù)為2、NaClO的系數(shù)為3,再根據(jù)原子守恒配平后反應方程式為:2FeCl3+10NaOH+3NaClO═2Na2FeO4+9NaCl+5H2O,NaClO是氧化劑,
故答案為:2、10、3、2、9、5;NaClO;
所含元素化合價降低的反應物是氧化劑;
(5)加入飽和KOH溶液可以增大K+的濃度,減小高鐵酸鉀的溶解,促進高鐵酸鉀晶體析出,
故答案為:減小高鐵酸鉀的溶解,促進高鐵酸鉀晶體析出;
(6)溶液中c(Fe3+)=5mol/L,根據(jù)Ksp[Fe(OH)3]=c(Fe3+)×c3(OH-)=4.0×10-38,可知開始沉淀時c(OH-)=2×10-13mol/L,則溶液中c(H+)=$\frac{10{\;}^{-14}}{2×10{\;}^{-13}}$mol/L=0.05mol/L,根據(jù)稀釋定律,需要鹽酸的體積$\frac{0.05mol/L×100mL}{2mol/L}$=2.5mL,
故答案為:2.5.
點評 本題考查原電池工作原理、物質(zhì)制備工藝流程,側(cè)重考查物質(zhì)制備方法的分析應用,掌握物質(zhì)性質(zhì)和平衡移動原理以及化學電池工作原理是解題關(guān)鍵,(1)中電極反應式書寫為難點,題目應該給出一定的信息,題目難度中等.


 小學奪冠AB卷系列答案
小學奪冠AB卷系列答案 ABC考王全優(yōu)卷系列答案
ABC考王全優(yōu)卷系列答案科目:高中化學 來源: 題型:實驗題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
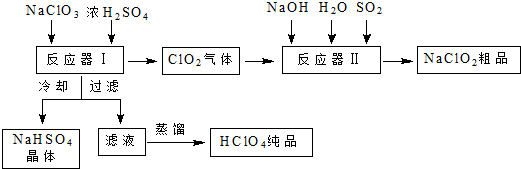
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 砷(As)是第四周期第VA族元素,它在自然界中的含量不高,但人類認識它、研究它的歷史卻很長.
砷(As)是第四周期第VA族元素,它在自然界中的含量不高,但人類認識它、研究它的歷史卻很長.查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
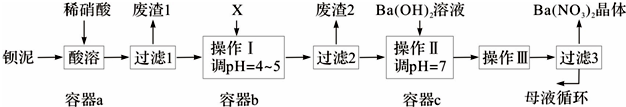
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
 甲烷在一定條件下可生成以下微粒:
甲烷在一定條件下可生成以下微粒:查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | p=$\frac{17V+22400}{22.422.4V}$ | B. | W=$\frac{17c}{ρ}$ | ||
| C. | $\frac{17V}{17V+22400}$=W | D. | C=$\frac{1000Vρ}{17V+22400}$ |
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權(quán)舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com