
| A. | N2(g)+3H2(g)?2NH3(g)△H=-92.0 kJ•mol-1,吸收的能量為46.0 kJ,則形成N-H鍵的數目為3NA | |
| B. | 常溫下,向一密閉容器中加入2molNO與1molO2,容器中的分子數目小于2NA | |
| C. | 18gD2O(2H2O)中,含有的中子總數為10NA | |
| D. | 1.0mol•L-1NaCl溶液中含有NA個Cl- |
分析 A.該反應為放熱反應,不是吸熱反應,吸收能量應該為斷裂氮氫鍵;
B.部分二氧化氮轉化成四氧化二氮,導致分子數減少;
C.重水的摩爾質量為20g/mol,重水分子中含有10個電子;
D.缺少氯化鈉溶液的體積,無法計算氯離子數目.
解答 解:A.N2(g)+3H2(g)?2NH3(g)△H=-92.0 kJ•mol-1,該反應為放熱反應,吸收能量應該斷裂氮氫鍵,故A錯誤;
B.常溫下,向一密閉容器中加入2molNO與1molO2,完全反應生成2mol二氧化氮,由于部分二氧化氮轉化成四氧化二氮,則容器中的分子數目小于2NA,故B正確;
C.18gD2O(2H2O)的物質的量為:$\frac{18g}{20g/mol}$=0.9mol,0.9mol重水分子中含有9mol中子,含有的中子總數為9NA,故C錯誤;
D.沒有告訴氯化鈉溶液的體積,無法計算溶液中氯離子的物質的量及數目,故D錯誤;
故選B.
點評 本題考查阿伏加德羅常數的應用,題目難度中等,注意掌握以物質的量為中心的各化學量與阿伏加德羅常數的關系,準確弄清分子、原子、原子核內質子中子及核外電子的構成關系,D為易錯點,注意題中缺少溶液體積.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:解答題
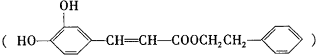 是一種天然抗癌藥物,在一定條件下能發生如下轉化
是一種天然抗癌藥物,在一定條件下能發生如下轉化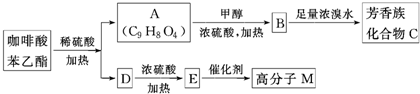
 ;
; ;
;查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 標準狀況下,22.4L苯的分子數約為NA個 | |
| B. | 常溫常壓下,7.0g乙烯與丙烯的混合物中含有氫原子的數目為NA | |
| C. | 100mL1mol/LCH3COOH溶液跟足量鈉反應,生成的氫氣分子數為0.05NA | |
| D. | 常溫下,在1molC5H12中含有共價鍵數15NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | wx mol-1 | B. | 22.4x mol-1 | C. | $\frac{22.4x}{ω}$mol-1 | D. | $\frac{11.2x}{ω}$mol-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | SiO2能和水發生化合反應生成硅酸 | |
| B. | SiO2是酸性氧化物,它不溶于任何酸 | |
| C. | SiO2的俗名叫水玻璃,不溶于水 | |
| D. | SiO2又叫水晶,能溶于NaOH溶液中 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ${\;}_{53}^{125}I$是碘的一種核素 | |
| B. | ${\;}_{53}^{125}I$核內的中子數與核外電子數之差為19 | |
| C. | ${\;}_{53}^{125}I$質量數為l25 | |
| D. | ${\;}_{53}^{125}I$是一種新發現的元素 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Cl2與NaOH溶液反應:Cl2+2OH-═Cl-+ClO-+H2O | |
| B. | 澄清石灰水與少量蘇打溶液混合:Ca2++OH-+HCO3-═CaCO3↓+H2O | |
| C. | 碳酸鈣溶于鹽酸:CaCO3+2H+═Ca2++CO2↑+H2O | |
| D. | 氯化亞鐵溶液中通入氯氣:2Fe2++Cl2═2Fe3++2Cl- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 標準狀況下,22.4L苯的分子數約為NA個 | |
| B. | 常溫常壓下,7.0g乙烯與丙烯的混合物中含有氫原子的數目為NA | |
| C. | 100 mL 1 mol/L CH3COOH溶液跟足量鈉反應,生成的氫氣分子數為0.05 NA | |
| D. | 常溫下,在1moLC5H12中含有共價鍵數15NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ac | B. | be | C. | df | D. | gh |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com