
| c2(CO) |
| c(CO2) |
| c2(CO) |
| c(CO2) |
| c2(CO) |
| c(CO2) |
| c(CO)c(H2) |
| c(H2O) |
| c(CO)c(H2O) |
| c(CO2)c(H2) |
| c2(CO) |
| c(CO2) |
| c2(SO3) |
| c2(SO2)c(O2) |
| 0��82 |
| 0��22��0.6 |



| �꼉 | �����n�� | �꼉 | �����n�� |
| ��һ | ��һ���M�n�����]�� | ��һ | ��һ���M�n�����]�� |
| �߶� | �߶����M�n�����]�� | ���� | �������M�n�����]�� |
| ���� | �������M�n�����]�� | ���� | �������M�n�����]�� |
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�
| c2(CO) |
| c(CO2) |
| c2(CO) |
| c(CO2) |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ��2013�ú���ʡ�����з�У�߶��όW(xu��)�����п�ԇ���W(xu��)ԇ�� �}�ͣ�����}
(12��)���W(xu��)ƽ��ԭ���ڹ��r(n��ng)�I(y��)���a(ch��n)�аl(f��)�]����Ҫ��ָ��(d��o)���á�
(1)����(y��ng)C(s)+CO2(g)
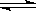 2CO(g)ƽ�ⳣ��(sh��)K�ı��_(d��)ʽ��
��
2CO(g)ƽ�ⳣ��(sh��)K�ı��_(d��)ʽ��
��
��֪C(s) +
H2O(g)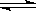 CO(g)+H2(g)��ƽ�ⳣ��(sh��)��K1��H2(g)��CO2(g)
CO(g)+H2(g)��ƽ�ⳣ��(sh��)��K1��H2(g)��CO2(g) 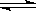 CO(g)��H2O(g)��ƽ�ⳣ��(sh��)��K2 ���tK�cK1��K2���ߵ��P(gu��n)ϵ��
��
CO(g)��H2O(g)��ƽ�ⳣ��(sh��)��K2 ���tK�cK1��K2���ߵ��P(gu��n)ϵ��
��
(2) ��֪ij�ض��£�����(y��ng)2SO2+O2 2SO3����ƽ�ⳣ��(sh��)K=19
2SO3����ƽ�ⳣ��(sh��)K=19
��ԓ�ض��µ��w�e�̶������]�����г���C(SO2)=1mol��L��1��C(O2)=1 mol��L��1����(d��ng)����(y��ng)��ԓ�ض���SO2�D(zhu��n)���ʞ�80���r��ԓ����(y��ng) (��ǡ���)�_(d��)�����W(xu��)ƽ���B(t��i)����δ�_(d��)������ (�������(y��ng)�����淴��(y��ng)��) �����M(j��n)�С�
(3)���ڿ��淴��(y��ng)��aA(g) +bB(g) cC(g)+dD(g)
��H = a kJ��mol-1��
cC(g)+dD(g)
��H = a kJ��mol-1��
��a+b��c+d������ƽ����_______(�������(y��ng)�����淴��(y��ng)��)�����Ƅӣ������ߜضȣ�ƽ�����淴��(y��ng)�����Ƅӣ��ta_______0(���������)
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ��2012-2013�W(xu��)�����ʡ��h������^(q��)����·�ЌW(xu��)�߶����ϣ����л��W(xu��)ԇ���������棩 �}�ͣ�����}
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ��2012-2013�W(xu��)����Cʡ�m��һ�и߶����ϣ����л��W(xu��)ԇ�������ƣ��������棩 �}�ͣ�����}
�鿴�𰸺ͽ���>>
�ٶ����� - ����(x��)���б� - ԇ�}�б�
����ʡ��(li��n)�W(w��ng)�`���Ͳ�����Ϣ�e��ƽ�_ | �W(w��ng)���к���Ϣ�e�^(q��) | ����p�_�e�^(q��) | ��vʷ̓�o���x�к���Ϣ�e�^(q��) | �����֙�(qu��n)�e�^(q��)
�`���Ͳ�����Ϣ�e���Ԓ��027-86699610 �e���]�䣺58377363@163.com