
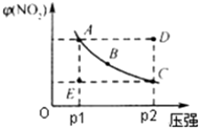
| A、abc | B、e | C、cd | D、d |


科目:高中化學 來源: 題型:
| A、Zn2+、Fe3+、Cu |
| B、Cu2+、Fe3+、Zn |
| C、Zn2+、Cu2+、Fe2+、Fe |
| D、Zn2+、Fe2+、Cu2+、Cu |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、1000mL,212g |
| B、950mL,543.4g |
| C、1000mL,572g |
| D、500mL,286g |
查看答案和解析>>
科目:高中化學 來源: 題型:
A、質量數為35的氯原子:
| ||
B、BaSO4的電離方程式:BaSO4=Ba2++S
| ||
| C、乙烯的結構簡式:C2H4 | ||
D、氯原子結構示意圖: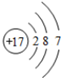 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、28.58kJ |
| B、82.16 kJ |
| C、53.58 kJ |
| D、89.3 kJ |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、②③⑤⑥ | B、①④ |
| C、只有①④ | D、只有②③⑤ |
查看答案和解析>>
科目:高中化學 來源: 題型:
| 1 |
| 4 |
| 1 |
| 2 |
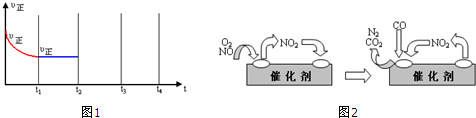
查看答案和解析>>
科目:高中化學 來源: 題型:
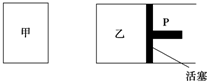
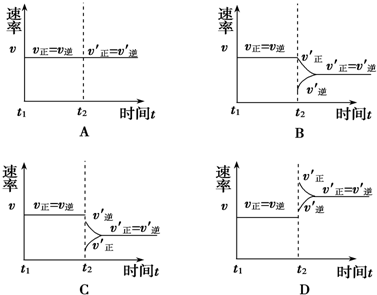
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com