
如圖所示的裝置或操作正確的是()
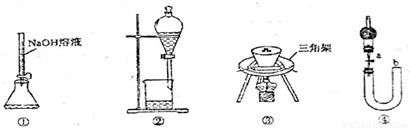
A.用裝置①量取15.00mL的NaOH溶液
B.用裝置②分離苯和水的混合物,苯應從下口流出
C.用裝置③陶瓷坩堝高溫煅燒CaCO3固體
D.關閉活塞a,從b處加水,以檢查裝置④的氣密性
科目:高中化學 來源:2016屆海南省高三臨考模擬化學試卷(解析版) 題型:選擇題
下列指定反應的離子方程式正確的是
A.向NaAlO2溶液中通入過量CO2:CO2+AlO2-+2H2O=Al(OH)3?+HCO3-
B.NH4HCO3溶液中加過量NaOH溶液并加熱:NH4++OH- NH3?+H2O
NH3?+H2O
C.用CH3COOH溶解CaCO3:CaCO3+2H+=Ca2++H2O+CO2?
D.Cu溶于稀硝酸HNO3:Cu+2H++NO3-=Cu2++NO?+H2O
查看答案和解析>>
科目:高中化學 來源:2016屆貴州省高三5月高考模擬理綜化學試卷(解析版) 題型:實驗題
實驗室從含碘廢液(除H2O外,含有CCl4、I2、I-等)中回收碘,其實驗過程如下:

(1)向含碘廢液中加入稍過量的Na2SO3溶液,將廢液中的I2還原為I-,其離子方程式為____________,該操作將I2還原為I-的目的是____________;
(2)操作X的名稱為____________;
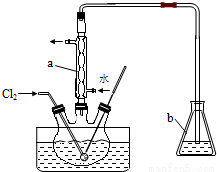
(3)氧化時,在三頸燒瓶中將含I-的水溶液用鹽酸調至pH約為2,緩慢通入Cl2,在40℃左右反應(實驗裝置如圖所示).實驗室控制在較低溫度下進行的原因是____________;儀器b中盛放的溶液為_____。
(4)已知:5SO32-+2IO3-+2H+═I2+5SO42-+H2O
某含碘廢水(pH約為8)中一定存在I2,可能存在I-、IO3-中的一種或兩種,請補充完整檢驗含碘廢水中是否含有I-、IO3-的實驗方案:(實驗中可供選擇的試劑:稀鹽酸、淀粉溶液、FeCl3溶液、Na2SO3溶液)。
①取適量含碘廢水用CCl4多次萃取、分液,直到水層用淀粉溶液檢驗不出有碘單質存在:
②____________;
③另從水層取少量溶液,加入1-2mL淀粉試液,加鹽酸酸化,滴加Na2SO3溶液,若溶液變藍色,說明廢水中含有IO3-,否則說明廢水中不含IO3-。
(5)二氧化氯(ClO2,黃綠色易溶于水的氣體)是高效、低毒的消毒劑和水處理劑。現用ClO2氧化酸性含I-廢液回收碘。
①完成ClO2氧化I-的離子方程式:□ClO2+□I-+□____________=□I2+□Cl-+□____________
②若處理含I-相同量的廢液回收碘,所需Cl2的物質的量是ClO2的____________倍
查看答案和解析>>
科目:高中化學 來源:2015-2016學年湖北省高二5月月考化學試卷(解析版) 題型:選擇題
NO2、O2和熔融KNO3可制作燃料電池,其原理如圖,該電池在使用過程中石墨I電極上生成氧化物Y,Y可循環使用。下列說法正確的是( )

A.O2在石墨Ⅱ附近發生氧化反應
B.該電池放電時NO3-向石墨Ⅱ電極遷移
C.石墨Ⅰ附近發生的反應:3NO2+2e-=NO+2NO3-
D.相同條件下,放電過程中消耗的NO2和O2的體積比為4:1
查看答案和解析>>
科目:高中化學 來源:2015-2016學年湖北省高二5月月考化學試卷(解析版) 題型:選擇題
下列實驗的現象及結論不正確的是( )
A.過氧化鈉放置在空氣中,最終轉變為白色粉末Na2CO3
B.SO2通入BaCl2溶液中產生白色沉淀BaSO3
C.打磨過的鋁箔和未打磨的鋁箔分別在空氣中灼燒,兩種鋁箔均熔化但不滴落,說明氧化鋁熔點比鋁高
D.分別向等物質的量濃度的Na2CO3和NaHCO3溶液中滴加酚酞,溶液都變紅,Na2CO3溶液紅色較深,說明Na2CO3水解程度大于NaHCO3
查看答案和解析>>
科目:高中化學 來源:2015-2016學年湖北省高二5月月考化學試卷(解析版) 題型:選擇題
某實驗報告記錄了如下數據,其中數據合理的是()
A.用溫度計測量出酒精的沸點為78.5℃
B.用50mL量筒量取23.00 mL濃鹽酸
C.用廣泛pH試紙測得氯水的pH值為2.1
D.用托盤天平稱量氧化銅粉末為11.70g
查看答案和解析>>
科目:高中化學 來源:2015-2016學年廣東省汕頭市高二下期末化學試卷(解析版) 題型:選擇題
設NA為阿伏伽德羅常數的值,下列說法正確的是
A.14 g乙烯和丙烯的混合物中總原子數為2NA個
B.在1mol的CH5+中所含的電子數為10NA
C. 16g CH4與18 g NH4+所含質子數相等
D.11.2 L的甲烷氣體含有甲烷分子數一定為0.5NA個
查看答案和解析>>
科目:高中化學 來源:2015-2016學年廣東省汕頭市高二下期末化學試卷(解析版) 題型:選擇題
下列實驗能夠獲得成功的是
A.檢驗溴乙烷中的溴:取溴乙烷加氫氧化鈉溶液,加熱,再加硝酸銀溶液有淺黃色沉淀生成.
B.檢驗葡萄糖:在硝酸銀溶液中滴加稀氨水至沉淀恰好溶解再加少許葡萄糖溶液,水浴加熱
C.檢驗乙醛:取2%硫酸銅溶液2 mL再加入2% NaOH溶液1mL,再加入少量乙醛加熱至沸騰.
D.實驗室制乙烯:取濃硫酸和乙醇體積比1:3的溶液迅速升溫至170℃
查看答案和解析>>
科目:高中化學 來源:2015-2016學年遼寧省高一下期中化學試卷(解析版) 題型:填空題
磷酸鐵鋰動力電池的正極與負極中間是聚合物的隔膜隔開的,鋰離子可以通過。該電池的總反應式為:Li1﹣xFePO4+LixC6═C6+LiFePO4 (注:LixC6是單質Li附在碳電極上的一種形式)
(1)磷酸鐵鋰電池放電時,負極反應式為 。
(2)若用該電池電解精煉銅,陰極質量增重19.2g時,則電池中通過聚合物隔膜的Li+數目為 。
(3)以該電池為電源,用Fe2O3為陽極,石墨為陰極,NaOH溶液為電解質溶液制備高鐵酸鈉(Na2FeO4),寫出陽極的電極反應式 。
(4)以該電池為電源,用惰性電極電解2L硫酸銅和氯化鈉的混合溶液, 若兩極均產生0.14mol氣體,電路中共有0.4mol的電子轉移,則電解后溶液的c(OH-)為 。
若兩極均產生0.14mol氣體,電路中共有0.4mol的電子轉移,則電解后溶液的c(OH-)為 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com