


科目:高中化學 來源: 題型:
| A、1.2mol/L |
| B、2 mol/L |
| C、0.2 mol/L |
| D、0.4mol/L |
查看答案和解析>>
科目:高中化學 來源: 題型:

查看答案和解析>>
科目:高中化學 來源: 題型:
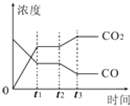 Ⅰ、對于反應CO(g)+H2O(g)?H2(g)+CO2(g)
Ⅰ、對于反應CO(g)+H2O(g)?H2(g)+CO2(g)| 溫度/℃ | 400 | 500 | 830 |
| 平衡常數K | 10 | 9 | 1 |
| 實驗編號 | n(CO) | n(H2O) | n(H2) | n(CO2) |
| A | 1 | 5 | 2 | 3 |
| B | 2 | 2 | 1 | 1 |
| C | 0.5 | 2 | 1 | 1 |
2- 7 |
2- 7 |
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
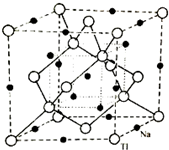 太陽能電池是通過光電效應或者光化學效應直接把光能轉化成電能的裝置.其材料除單晶硅,還有銅銦鎵硒等化合物.
太陽能電池是通過光電效應或者光化學效應直接把光能轉化成電能的裝置.其材料除單晶硅,還有銅銦鎵硒等化合物.查看答案和解析>>
科目:高中化學 來源: 題型:
| 1 |
| 2 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、化合物電離出的陽離子有氫離子的就是酸 | ||
| B、化合物電離出的陰離子有氫氧根離子的就是堿 | ||
| C、鹽電離出的陽離子不一定都是金屬陽離子 | ||
D、NH4Cl電離的電離方程式是NH4Cl═NH
|
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com