

 ,X在一定條件下能發生的反應是acd(選填字母);
,X在一定條件下能發生的反應是acd(選填字母);
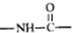
 ,貝諾酯的結構簡式是
,貝諾酯的結構簡式是
 用鄰甲基苯酚可以合成有機物X.合成路線如圖:鄰甲基苯酚→W→X的結構簡則W的結構簡式是
用鄰甲基苯酚可以合成有機物X.合成路線如圖:鄰甲基苯酚→W→X的結構簡則W的結構簡式是 .
. .
. 分析 (1)有機物X分子式為C9H8O4,結合其紅外光譜圖可知,X含有苯環、-OOCCH3、-COOH,核磁共振氫譜圖峰面積比是1:1:1:1:1:3,故X為 ;
;
(2)水楊酸( )能與化合物Y在一定條件發生取代反應生成X與乙酸,則Y為乙酸酐;
)能與化合物Y在一定條件發生取代反應生成X與乙酸,則Y為乙酸酐;
(3)有關撲熱息痛的信息如下:①分子中含有基團 ,②苯環上的一溴代物只有兩種,③能和濃溴水反應生成白色沉淀,含有酚羥基,④能發生水解反應生成乙酸,結合①可知含有-NHCOCH3,結合②可知,-OH與-NHCOCH3處于對位;
,②苯環上的一溴代物只有兩種,③能和濃溴水反應生成白色沉淀,含有酚羥基,④能發生水解反應生成乙酸,結合①可知含有-NHCOCH3,結合②可知,-OH與-NHCOCH3處于對位;
(4)鄰甲基苯酚與乙酸酐反應得到W,然后在用酸性高錳酸鉀溶液氧化得到X;
(5)芳香族化合物Q和X的分子式相同,Q具有下列性質:①能和NaHCO3反應,說明含有-COOH,②能水解且能發生銀鏡反應,還含有-OOCH,含有1個側鏈為-CH(COOH)OOCH,含有2個側鏈為-CH2COOH、-OOCH,或-COOH、-CH2OOCH,含有3個側鏈為-CH3、-COOH、-OOCH.
解答 解:(1)有機物X分子式為C9H8O4,結合其紅外光譜圖可知,X含有苯環、-OOCCH3、-COOH,核磁共振氫譜圖峰面積比是1:1:1:1:1:3,故X為 ,可以發生加成反應、酯化反應、水解反應,不能發生消去反應,
,可以發生加成反應、酯化反應、水解反應,不能發生消去反應,
故答案為: ;acd;
;acd;
(2)水楊酸( )能與化合物Y在一定條件發生取代反應生成X與乙酸,則Y為乙酸酐,反應方程式為:
)能與化合物Y在一定條件發生取代反應生成X與乙酸,則Y為乙酸酐,反應方程式為: ,
,
故答案為: ;
;
(3)有關撲熱息痛的信息如下:①分子中含有基團 ,②苯環上的一溴代物只有兩種,③能和濃溴水反應生成白色沉淀,含有酚羥基,④能發生水解反應生成乙酸,結合①可知含有-NHCOCH3,結合②可知,-OH與-NHCOCH3處于對位,撲熱息痛的結構簡式是:
,②苯環上的一溴代物只有兩種,③能和濃溴水反應生成白色沉淀,含有酚羥基,④能發生水解反應生成乙酸,結合①可知含有-NHCOCH3,結合②可知,-OH與-NHCOCH3處于對位,撲熱息痛的結構簡式是: ,lmol貝諾酯與lmol水可以生成lmolX和lmol撲熱息痛,貝諾酯的結構簡式是:
,lmol貝諾酯與lmol水可以生成lmolX和lmol撲熱息痛,貝諾酯的結構簡式是: ,
,
故答案為: ;
; ;
;
(4)鄰甲基苯酚與乙酸酐反應得到W,然后在用酸性高錳酸鉀溶液氧化得到X,則W的結構簡式為: ,
,
故答案為: ;
;
(5)芳香族化合物Q和X的分子式相同,Q具有下列性質:①能和NaHCO3反應,說明含有-COOH,②能水解且能發生銀鏡反應,還含有-OOCH,含有1個側鏈為-CH(COOH)OOCH,含有2個側鏈為-CH2COOH、-OOCH,或-COOH、-CH2OOCH,各有鄰、間、對三種,含有3個側鏈為-CH3、-COOH、-OOCH,-CH3、-COOH處于鄰位時,-OOCH有4種位置,-CH3、-COOH處于間位時,-OOCH有4種位置,-CH3、-COOH處于對位時,-OOCH有2種位置,故符合條件的Q的結構有:1+3+3+4+4+2=17種,苯環上只有一個取代基的異構體的結構簡式為 ,
,
故答案為:17; .
.
點評 本題考查有機物的推斷與合成、限制2條件同分異構體的書寫,側重考查學生分析推理能力,難度中等.


科目:高中化學 來源: 題型:選擇題
| A. | 2:3 | B. | 2:5 | C. | 2:7 | D. | 7:2 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 加入SO3 | B. | 壓強不變,充入Ar | C. | 容積不變,充入Ar | D. | 降低溫度 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 分子式為C9H5O4 | |
| B. | 與溴水既能發生取代反應,又能發生加成反應 | |
| C. | 1mol咖啡酸最多可與5mol氫氣發生加成反應 | |
| D. | 能與Na2CO3溶液反應,但不能與NaHCO3溶液反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 執行“限塑令”主要是為了節約資源 | |
| B. | 金剛石是自然界中硬度最大的物質,不可能與氧氣發生反應 | |
| C. | 利用丁達爾效應可區分蛋白質溶液與葡萄糖溶液 | |
| D. | 工業生產硫酸中,建立高煙囪可以降低地面SO2的濃度,減少空氣污染 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

 .
.
 +CaCl2+H2O
+CaCl2+H2O
| 實驗編號 | 試管Ⅰ中試劑 | 試管Ⅱ中 試劑 | 有機層的 厚度/cm |
| A | 2mL乙醇、1mL乙酸、1mL18mol•L-1 濃硫酸 | 飽和Na2CO3 溶液 | 3.0 |
| B | 2mL乙醇、1mL乙酸 | 0.1 | |
| C | 2mL乙醇、1mL乙酸、3mL 2mol•L-1 H2SO4 | 0.6 | |
| D | 2mL乙醇、1mL乙酸、鹽酸 | 0.6 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com