
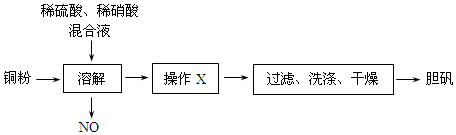
分析 (1)銅粉與稀硫酸、稀硝酸反應生成硫酸銅溶液,如得到膽礬,應將溶液進行蒸發濃縮、冷卻結晶操作,然后經過濾、洗滌、干燥可得到晶體;過濾需要用到的玻璃儀器有漏斗、燒杯、玻璃棒;
(2)NO與空氣、H2O反應生成硝酸,結合質量守恒平衡方程式.
(3)計算CuO、Cu的質量,結合銅元素質量守恒可計算CuSO4•5H2O的質量;結合反應的離子方程式計算原混合液中硫酸和硝酸的物質的量之比.
解答 解:(1)銅粉與稀硫酸、稀硝酸反應生成硫酸銅溶液,如得到膽礬,應將溶液進行蒸發濃縮、冷卻結晶操作,然后經過濾、洗滌、干燥可得到晶體;過濾需要用到的玻璃儀器有漏斗、燒杯、玻璃棒;
故答案為:蒸發濃縮、冷卻結晶;漏斗、燒杯、玻璃棒;
(2)NO與空氣、H2O反應生成硝酸,反應的方程式為4NO+3O2+2H2O=4HNO3;
故答案為:4NO+3O2+2H2O=4HNO3;
(3)①n(CuO)=48g×20%÷80g/mol=0.12mol,n(Cu)=48g×(1-20%)÷64g/mol=0.6mol,則n(CuSO4•5H2O)=0.12mol+0.6mol=0.72mol,m(CuSO4•5H2O)=0.72mol×250g/mol=180g;
故答案為:180 g;
②發生反應:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
n(HNO3)=$\frac{0.6mol}{3}×2$=0.4mol,n(H2SO4)=n(CuSO4•5H2O)=0.72mol,
則n(H2SO4):n(HNO3)=0.72mol:0.4mol=9:5;
故答案為:9:5.
點評 本題考查物質的分離、提純的實驗綜合應用,為高頻考點,側重于學生的分析能力、實驗能力和計算能力的考查,主要把握實驗的原理、操作方法以及守恒法應用于化學方程式的計算,難度中等.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:選擇題
| A. | 在鍍件上電鍍銅時,可用金屬銅作陽極 | |
| B. | 鍍層破損后,白鐵(鍍鋅)比馬口鐵(鍍錫)更易被腐蝕 | |
| C. | 工業上電解飽和食鹽水制燒堿,NaOH在陰極產生 | |
| D. | 鋼鐵在發生析氫腐蝕和吸氧腐蝕時,完全相同的反應是負極反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 2.12 g | B. | 4.24 g | C. | 3.18 g | D. | 5.28 g |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
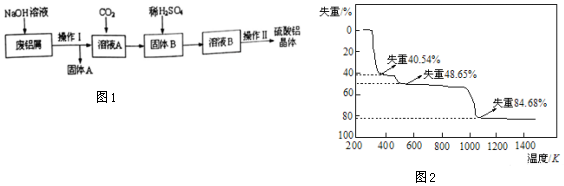
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 每當固體質量減輕5.6g時,生成2.8g Si | |
| B. | 氧化劑和還原劑的物質的量之比為1:2 | |
| C. | 硅單質在常溫下不與任何酸、堿反應 | |
| D. | 單質硅與單質碳均具有一定的還原性 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
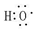 ;
; 查看答案和解析>>
科目:高中化學 來源: 題型:解答題
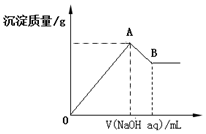 在含有0.60molCl-、0.80molSO42-及一定量Mg2+和Al3+的混合溶液中,滴入一定濃度NaOH溶液,產生沉淀情況如圖(不考慮Mg2+和Al3+水解及水電離對離子數目的影響).若反應前Al3+的物質的量為a mol,Al3+的物質的量與混合溶液中離子總物質的量的比值為x.
在含有0.60molCl-、0.80molSO42-及一定量Mg2+和Al3+的混合溶液中,滴入一定濃度NaOH溶液,產生沉淀情況如圖(不考慮Mg2+和Al3+水解及水電離對離子數目的影響).若反應前Al3+的物質的量為a mol,Al3+的物質的量與混合溶液中離子總物質的量的比值為x.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ${\;}_{\;}^{1}$H(氕)、${\;}_{\;}^{2}$H(氘)、${\;}_{\;}^{3}$H(氚)是三種氫元素 | |
| B. | 所有氫元素粒子的核外都只有一個電子 | |
| C. | 所有氫元素粒子的化學性質都相同 | |
| D. | 能用符號H表示的原子在元素周期表中的位置相同 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 乙烯和甲烷都能發生加成反應 | |
| B. | 米酒變酸是因為乙醇被氧化為乙酸 | |
| C. | 糖類、油脂、蛋白質都屬于天然高分子化合物 | |
| D. | 可用熱的NaOH溶液除去乙酸乙酯中的乙酸雜質 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com