
德國著名行業雜志《應用化學》上曾刊登文章介紹:某中德聯合研究小組設計制造了一種“水瓶”,用富勒烯(C60)的球形籠子作“瓶體”,一種磷酸鹽作“瓶蓋”,恰好可將一個水分子關在里面。下列說法正確的是( )。
A.水、雙氧水、水玻璃都是純凈物
B.石墨和C60互為同素異形體
C.磷酸鈣中所含元素都是短周期元素
D.一定條件下石墨轉化為C60是化學變化
 期末金牌卷系列答案
期末金牌卷系列答案 輕松課堂標準練系列答案
輕松課堂標準練系列答案科目:高中化學 來源:2013-2014學年高考化學二輪復習江蘇專用 第7講水溶液中的離子平衡練習卷(解析版) 題型:選擇題
25 ℃時,用濃度為0.100 0 mol·L-1的NaOH溶液滴定20.00 mL濃度均為0.100 0 mol·L-1的三種酸HX、HY、HZ,滴定曲線如圖所示。下列說法正確的是( )。

A.在相同溫度下,同濃度的三種酸溶液的導電能力順序:HZ<HY<HX
B.根據滴定曲線,可得Ka(HY)≈10-5
C.將上述HX、HY溶液等體積混合后,用NaOH溶液滴定至HX恰好完全反應時:c(X-)>c(Y-)>c(OH-)>c(H+)
D.HY與HZ混合,達到平衡時c(H+)=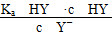 +c(Z-)+c(OH-)
+c(Z-)+c(OH-)
查看答案和解析>>
科目:高中化學 來源:2013-2014學年高考化學二輪復習江蘇專用 第4講物質結構元素周期律練習卷(解析版) 題型:選擇題
X、Y是元素周期表中ⅦA族的兩種元素,下列能說明X的非金屬性比Y強的是( )。
A.電子層數:X>Y
B.氣態氫化物的穩定性:HX<HY
C.酸性:HXO4>HYO4
D.能發生置換反應:Y2+2NaX=X2+2NaY
查看答案和解析>>
科目:高中化學 來源:2013-2014學年高考化學二輪復習江蘇專用 第2講化學常用計量練習卷(解析版) 題型:選擇題
現取m g鎂鋁合金在一定濃度的稀硝酸中恰好完全溶解(硝酸的還原產物只有NO),向反應后的混合溶液中滴加b mol·L-1 NaOH溶液,當滴加到V mL時,得到沉淀質量恰好為最大值n g,則下列有關該實驗的說法中正確的有( )。
①沉淀中OH-的質量為(n-m)g
②恰好溶解后溶液中的NO3—的物質的量為 mol
mol
③反應過程中轉移的電子數為 mol
mol
④標準狀況下生成NO的體積為  L
L
⑤與合金反應的硝酸的物質的量為( +
+ )mol
)mol
A.5項 B.4項 C.3項 D.2項
查看答案和解析>>
科目:高中化學 來源:2013-2014學年高考化學二輪復習江蘇專用 第2講化學常用計量練習卷(解析版) 題型:選擇題
如圖所示,兩個連通容器用活塞分開,左右兩室體積相同,左室充入一定量NO,右室充入一定量O2,且恰好使兩容器內氣體密度相同。打開活塞,使NO與O2充分反應,下列判斷正確的是(不考慮NO2轉化為N2O4)

A.開始時左右兩室中的分子數相同
B.反應前后左室的壓強相同
C.反應后容器內的密度與反應前的相同
D.反應后容器內無O2存在
查看答案和解析>>
科目:高中化學 來源:2013-2014學年高考化學二輪復習江蘇專用 第1講物質的組成性質和分類練習卷(解析版) 題型:選擇題
下列有關說法錯誤的是( )。
A.通過化學反應無法生成新的同位素
B.NaCl水溶液導電、食品袋中生石灰吸水均為物理變化
C.鹽酸、氫氧化鐵膠體、汽油、橡膠均為混合物
D.生成鹽和水的反應不一定是中和反應
查看答案和解析>>
科目:高中化學 來源:2013-2014學年高考化學二輪復習江蘇專用 第15講實驗化學練習卷(解析版) 題型:實驗題
苯乙醚是一種無色油狀液體,熔點-30 ℃,沸點 172 ℃,不溶于水,易溶于醇和醚,廣泛用于有機合成中間體及制造醫藥、染料等。實驗合成的原理為:

主要實驗步驟如下:
(Ⅰ)合成:在燒瓶中(裝置如圖)加入7.53 g苯酚、3.92 g NaOH和4 mL水,開動攪拌器,使固體全部溶解,加熱反應器控制溫度80~90 ℃之間,并用滴液漏斗慢慢滴加8.59 mL溴乙烷(沸點38.4 ℃),大約40 min滴加完畢,繼續攪拌1 h,冷卻至室溫。

(Ⅱ)分離與提純。
①加入適量的水(10~15 mL)使固體完全溶解,將液體轉入分液漏斗中,分出水相;
②水相用8 mL乙醚萃取一次,與有機相合并;
③有機相用等體積飽和食鹽水洗兩次,分出水相,再將水相用6 mL乙醚萃取一次,與有機相合并;
④有機相用無水氯化鈣干燥;
⑤先用水浴蒸出乙醚,然后常壓蒸餾,收集148 ℃穩定的餾分得苯乙醚;
⑥稱量產品質量3.69 g。
回答下列問題:
(1)用圖示的滴液漏斗代替普通漏斗滴液,其優點是_______________________。
(2)合成時,開動攪拌器的目的是_______________________________。
(3)控制溫度80~90 ℃可采用的方法是________________,兩次用乙醚萃取的目的是________________________________________________________。
(4)蒸餾時最后溫度穩定在148 ℃左右,其原因是_________________
_______________________________________________________。
(5)本次產率為12.4%,產率偏低的原因可能有__________________________
______________________________________________。
查看答案和解析>>
科目:高中化學 來源:2013-2014學年高考化學二輪復習江蘇專用 第12講化學實驗基礎練習卷(解析版) 題型:實驗題
堿式碳酸銅是一種化工原料,化學式用mCu(OH)2·nCuCO3表示。實驗室以廢銅屑為原料制取堿式碳酸銅的步驟如下:

Ⅰ.廢銅屑制硝酸銅
方案1:將銅屑在空氣中充分灼燒,殘留固體溶于稀硝酸;
方案2:如圖1(夾持儀器已省略)。將濃硝酸緩慢加到廢銅屑中(廢銅屑過量),充分反應后過濾,得到硝酸銅溶液。
方案3:將方案2中濃硝酸換成稀硝酸,其他不變。
Ⅱ.堿式碳酸銅的制備
①向大試管中加入碳酸鈉溶液和硝酸銅溶液
②水浴加熱至70 ℃左右
③用0.4 mol·L-1的NaOH溶液調節pH至8.5,振蕩、靜置、過濾
④用熱水洗滌、烘干,得到堿式碳酸銅產品
請回答下列問題:
(1)按方案1實驗,必須選擇的下列儀器有________(填序號)。

(2)圖2中能分別替代圖1中B和C裝置的是________(填裝置序號)。
(3)已知:NO+NO2+2NaOH===2NaNO2+H2O;2NO2+2NaOH===NaNO3+NaNO2+H2O,NO不能單獨與NaOH溶液反應,實驗結束時,如何操作才能使裝置中的有毒氣體被NaOH溶液完全吸收?__________________________。
(4)步驟④中洗滌的目的是______________________________________。
(5)步驟③過濾后的濾液中含有CO32—,檢驗CO32—的方法是_________________________________________________________。
(6)測定堿式碳酸銅組成的方法主要有兩種:
方法1 灼燒法:取34.6 g純凈物mCu(OH)2·nCuCO3,在硬質試管里灼燒,將氣體產物依次通入足量的濃硫酸、足量的堿石灰中,完全吸收后濃硫酸凈增1.8 g,堿石灰凈增8.8 g。
方法2 還原法:在氫氣中加強熱,測反應前后固體的質量。
①利用上述數據推算堿式碳酸銅的化學式_____________________。
②配平化學方程式:mCu(OH)2·nCuCO3+________H2 ________Cu+________CO2↑+________H2O
________Cu+________CO2↑+________H2O
查看答案和解析>>
科目:高中化學 來源:2013-2014學年高考化學二輪復習提分訓練專題12物質結構與性質(選修)練習卷(解析版) 題型:選擇題
某元素的最外層電子數為2,價電子數為5,并且是同族中原子序數最小的元素,關于該元素的判斷錯誤的是( )。
A.電子排布式為1s22s22p63s23p63d34s2
B.該元素為V
C.該元素為ⅡA族元素
D.該元素位于d區
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com