
| 實驗編號 | HA物質的量濃度(mol•L-1) | NaOH物質的量濃度(mol•L-1) | 混合溶液的pH |
| ① | 0.1 | 0.1 | pH=9 |
| ② | c | 0.2 | pH=7 |
| ③ | 0.2 | 0.1 | pH<7 |
分析 (1)c在①組實驗中酸堿恰好完全反應生成鹽NaA,混合溶液呈堿性,說明NaA是強堿弱酸鹽,則HA是弱酸,酸或堿抑制水電離,含有弱離子的鹽促進水電離,且酸中氫離子濃度或堿中氫氧根離子濃度越大,其抑制水電離程度越大;
(2)HA是弱酸、NaOH是強堿,要使混合溶液呈中性,則酸應該稍微過量;
(3)③組實驗中溶質為等物質的量濃度的NaA和HA,混合溶液呈酸性,說明HA的電離程度大于酸根離子水解程度,再結合電荷守恒判斷離子濃度大小順序;
(4)常溫下,已知KSP[Cu(OH)2]=2×10-20,某CuSO4溶液里c(Cu2+)=0.02mol•L-1,如果要生成Cu(OH)2沉淀,溶液中c(OH-)>$\sqrt{\frac{{K}_{sp}[Cu(OH)_{2}]}{c(C{u}^{2+})}}$.
解答 解:(1)c在①組實驗中酸堿恰好完全反應生成鹽NaA,混合溶液呈堿性,說明NaA是強堿弱酸鹽,則HA是弱酸,酸或堿抑制水電離,含有弱離子的鹽促進水電離,且酸中氫離子濃度或堿中氫氧根離子濃度越大,其抑制水電離程度越大,0.1mol/L的HA溶液中氫離子濃度小于0.1mol/LNaOH溶液,所以NaOH抑制水電離程度大于HA,NaA促進水電離,
所以a、b、c由大到小的順序是c>a>b,
故答案為:cab;
(2)HA是弱酸、NaOH是強堿,要使混合溶液呈中性,則酸應該稍微過量,酸堿的體積相等,則酸濃度大于堿濃度,則c>0.2,故答案為:>;
(3)③組實驗中溶質為等物質的量濃度的NaA和HA,混合溶液呈酸性,說明HA的電離程度大于酸根離子水解程度,再結合電荷守恒得c(A-)>c(Na+),酸的電離及酸根離子水解程度都較小,則溶液中離子濃度大小順序為c(A-)>c(Na+)>c(H+)>c(OH-),
故答案為:c(A-)>c(Na+)>c(H+)>c(OH-);
(4)常溫下,已知KSP[Cu(OH)2]=2×10-20,某CuSO4溶液里c(Cu2+)=0.02mol•L-1,如果要生成Cu(OH)2沉淀,溶液中c(OH-)>$\sqrt{\frac{{K}_{sp}[Cu(OH)_{2}]}{c(C{u}^{2+})}}$=$\sqrt{\frac{2×1{0}^{-20}}{0.02}}$mol/L=10-9 mol/L,則溶液中c(H+)=10-5mol/L,溶液的pH=5,
故答案為:5.
點評 本題考查酸堿混合溶液定性判斷、難溶物溶解平衡等知識點,為高頻考點,側重考查學生分析判斷及計算能力,根據酸的強弱結合混合溶液酸堿性、電荷守恒及溶度積常數等知識點分析解答即可,題目難度不大.


科目:高中化學 來源: 題型:解答題
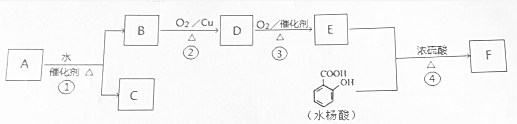
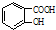 $→_{△}^{濃硫酸}$
$→_{△}^{濃硫酸}$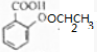 +H2O.
+H2O. $→_{△}^{濃硫酸}$
$→_{△}^{濃硫酸}$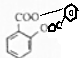 +H2O.
+H2O.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | A和B可能是同分異構體 | |
| B. | A和B不一定是同系物 | |
| C. | A和B完全燃燒后生成的水的質量相等 | |
| D. | A和B含碳的質量分數相同 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 乙醇和乙二醇屬于同系物 | |
| B. | 1-丁烯存在順反異構體 | |
| C. | 將苯加入溴水中,溴水褪色,是因為發生了加成反應 | |
| D. | 分子式為C3H8與C6H14的兩種有機物一定互為同系物 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 甲苯與溴水 | B. | 乙酸鈉溶液與硫酸 | ||
| C. | 甲苯與KMnO4酸性溶液 | D. | 甲酸溶液與銀氨溶液水浴共熱 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | C2H6與C3H8沒有同分異構體,CH2O2與C2H4O2屬于同系物 | |
| B. | 一定條件下,乙酸乙酯、淀粉、蛋白質、乙烯都能與水發生水解反應 | |
| C. | 一定條件下,完全燃燒14g含氧質量分數為a的乙烯、乙醛混合氣體,則生成水的質量為18(1-a)g | |
| D. | 全降解塑料( 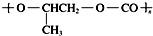 )可由單體環氧丙烷( )可由單體環氧丙烷(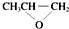 )和CO2縮聚制得 )和CO2縮聚制得 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 0.5Q | B. | Q | C. | 2Q | D. | 5Q |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 乙醇和乙酸都能與金屬鈉反應 | |
| B. | 用氫氧化鈉除去乙酸乙酯中的少量乙酸 | |
| C. | 植物油和動物脂肪都不能使溴水褪色 | |
| D. | 乙烯和聚乙烯都能使溴的四氯化碳溶液褪色 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com