
原子結構決定元素的性質,下列說法中正確的是
A. Na、Al、Cl的原子半徑依次減小,Na+、Al3+、Cl-的離子半徑也依次減小,
B. 在第ⅥA族元素的氫化物(H2R)中,熱穩定性最強的其沸點也一定最高
C. 第二周期元素的最高正化合價都等于其原子的最外層電子數
D. 非金屬元素的非金屬性越強,其氧化物對應水化物的酸性也一定越強
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:解答題
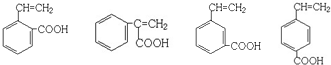
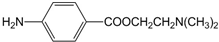 )的三條合成路線如下圖所示(部分反應試劑和條件已省略):
)的三條合成路線如下圖所示(部分反應試劑和條件已省略):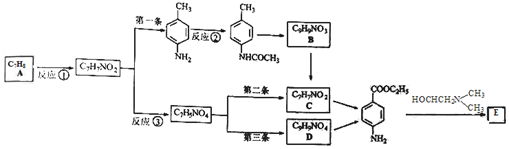
 ;C的名稱是對氨基苯甲酸.
;C的名稱是對氨基苯甲酸.
查看答案和解析>>
科目:高中化學 來源:2017屆江西省鷹潭市高三上學期第四次月考化學試卷 題型:選擇題
下列說法在一定條件下可以實現的是
①酸性氧化物與堿發生反應
②弱酸與鹽溶液反應可以生成強酸
③沒有水生成,也沒有沉淀和氣體生成的復分解反應
④兩種酸溶液充分反應后的溶液體系為中性
⑤有單質參加的非氧化還原反應⑥兩種氧化物反應的產物有氣體
A.①②③④⑤⑥
B.①②⑤⑥
C.①②③⑤
D.①②③⑤⑥
查看答案和解析>>
科目:高中化學 來源:2017屆吉林省長春市高三上學期期中考試化學試卷(解析版) 題型:推斷題
元素推斷題:
X、Y、Z、W為四種短周期元素,其中Y元素原子核外最外層電子數是其電子層數的3倍,它們在周期表中的相對位置如下圖所示:
X | Y |
|
| Z | W |
請回答下列問題:
(1)W位于周期表中第 周期,第 族。
(2)X可形成雙原子分子,其分子的電子式是 ;Y和氫元素形成的10電子微粒中常見的+1價陽離子為 (填化學式,下同);Z和氫元素形成的18電子微粒中常見的-1價陰離子為 。
(3)工業上將干燥的W單質通入熔融的Z單質中可制得化合物Z2W2,該物質可與水反應生成一種能使品紅溶液褪色的氣體,0.2mol該物質參加反應時轉移0.3mol電子,其中只有一種元素化合價發生改變,寫出Z2W2與水反應的化學方程式 。
(4)在一定條件下,由元素Y和Z組成的一種氣態化合物可發生催化氧化反應,反應達平衡進有三種氣態物質共存,已知每轉移4mol電子放熱190.0kJ,該反應的熱化學方程式為 。
查看答案和解析>>
科目:高中化學 來源:2017屆吉林省長春市高三上學期期中考試化學試卷(解析版) 題型:選擇題
已知:Kw=1.0×10-14,Al(OH)3 AlO2-+H++H2O,K=2.0×10-13。則Al(OH)3溶于NaOH溶液反應的平衡常數數值為
AlO2-+H++H2O,K=2.0×10-13。則Al(OH)3溶于NaOH溶液反應的平衡常數數值為
A.10
B.15
C.20
D.25
查看答案和解析>>
科目:高中化學 來源:2017屆吉林省長春市高三上學期期中考試化學試卷(解析版) 題型:選擇題
下列關于物質分類的說法正確的是
①稀豆漿、硅酸、氯化鐵溶液都屬于膠體
②HF、HI都屬于弱電解質
③Na2O、MgO、Al2O3均屬于堿性氧化物
④明礬、冰醋酸、四氧化三鐵都不是混合物
⑤葡萄糖、油脂都不屬于有機高分子化合物
A.④⑤
B.②④
C.①②
D.③⑤
查看答案和解析>>
科目:高中化學 來源:2017屆湖南省長沙市高三上學期第三次月考模擬化學試卷 題型:推斷題
(1)某透明溶液僅含Na+、Fe2+、Ba2+、Al3+、NO3-、Cl-、SO42-中的4種離子,所含離子均為1mol.若向該溶液中加入過量的稀硫酸,有氣泡產生,且溶液中陰離子種類不變(不考慮水的電離和離子的水解).回答下列問題:
①溶液中存在的離子是;
②寫出溶液中加入過量的稀硫酸反應的離子方程式.
(2)CNO-在酸性條件下繼續與NaClO反應生成N2、CO2、Cl2等,寫出CNO-在酸性條件下被NaClO氧化的離子方程式:________。
(3)酸性KMnO4、H2O2、NaClO在生產、生活、衛生醫療中常用作消毒劑,其中H2O2還可用于漂白,是化學實驗室里必備的重要氧化試劑。高錳酸鉀造成的污漬可用還原性的草酸(H2C2O4)去除,Fe(NO3)3也是重要氧化試劑,下面是對這三種氧化劑性質的探究。
①向浸泡銅片的稀鹽酸中加入H2O2后,銅片溶解,反應的化學方程式________________。
②取300mL0.2mol/L的KI溶液與一定量的酸性KMnO4溶液恰好反應,生成等物質的量的I2和KIO3,則消耗KMnO4的物質的量的是________mol。
③在Fe(NO3)3溶液中加入Na2SO3溶液,溶液先由棕黃色變為淺綠色,過一會又變為棕黃色。寫出溶液先變為淺綠色的離子方程式_________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
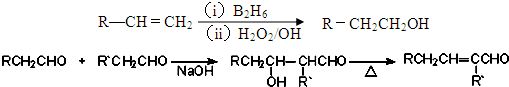
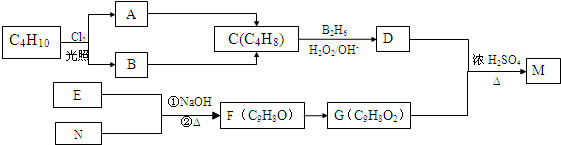
 、
、 ;
; .
.查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 微粒半徑:Cl->K+>Al3+>O2- | B. | 堿性:KOH>Ca(OH)2>Mg(OH)2 | ||
| C. | 晶體熔點:金剛石>氯化鎂>汞>碘 | D. | 穩定性和還原性:H2O>H2S>AsH3 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com